Sejarah kalori, bahagian, jenis dan ciri-ciri mereka
The calorimeter adalah peranti yang digunakan untuk mengukur perubahan suhu kuantiti bahan (biasanya air) haba spesifik yang diketahui. Perubahan suhu ini disebabkan oleh haba yang diserap atau dilepaskan dalam proses yang sedang dikaji; kimia jika reaksi, atau fizikal jika ia terdiri daripada fasa atau perubahan keadaan.
Di makmal, kalori paling mudah yang boleh didapati ialah cawan kopi. Ia digunakan untuk mengukur haba yang diserap atau dilepaskan dalam tindak balas pada tekanan tetap, dalam larutan akueus. Reaksi dipilih untuk mengelakkan campur tangan reagen atau produk gas.
 Dalam tindak balas eksotermik, jumlah haba yang dilepaskan dapat dikira dari peningkatan suhu kalorimeter dan larutan berair:
Dalam tindak balas eksotermik, jumlah haba yang dilepaskan dapat dikira dari peningkatan suhu kalorimeter dan larutan berair:
Jumlah haba yang dikeluarkan dalam reaksi = jumlah haba yang diserap oleh kalorimeter + jumlah haba yang diserap oleh larutan
Jumlah haba yang diserap oleh kalorimeter dipanggil kapasiti kalori calorimeter. Ini ditentukan dengan membekalkan haba yang diketahui kepada kalorimeter dengan jisim air tertentu. Kemudian, peningkatan suhu kalorimeter dan penyelesaiannya diukur.
Dengan data ini, dan penggunaan haba tertentu air (4.18 J / g.ºC), kapasiti kalori kalorimeter boleh dikira. Kapasiti ini juga dipanggil pemalar kalori.
Sebaliknya, haba yang diperolehi oleh larutan berair sama dengan m · ce · Δt. Dalam rumus m = jisim air, ce = haba spesifik air dan Δt = variasi suhu. Mengetahui semua ini, seseorang dapat mengira jumlah haba yang dikeluarkan oleh reaksi eksotermik.
Indeks
- 1 Sejarah calorimeter
- 2 Bahagian
- 3 Jenis dan ciri-ciri mereka
- 3.1 Cawan kopi
- 3.2 Pam kalorimetrik
- 3.3 Calorimeter adiabatik
- 3.4 Calorimeter isoperibolic
- 3.5 Calorimeter aliran
- 3.6 Calorimeter untuk kalori pengimbasan pembezaan
- 4 Aplikasi
- 4.1 Dalam fizikokimia
- 4.2 Dalam sistem biologi
- 4.3 Calorimeter pam oksigen dan kuasa kalori
- 5 Rujukan
Sejarah calorimeter
Pada tahun 1780, A. L. Lavoisier, ahli kimia Perancis, yang dianggap sebagai salah satu bapa kimia, menggunakan guinea pig untuk mengukur pengeluaran haba dengan pernafasannya.
Bagaimana? Menggunakan peranti yang serupa dengan kalori. Haba yang dihasilkan oleh babi guinea dibuktikan oleh pencairan salji yang mengelilingi radas.
Penyelidik A. L Lavoisier (1743-1794) dan P. S. Laplace (1749-1827) merancang calorimeter yang digunakan untuk mengukur haba spesifik badan dengan cara meleleh ais.
Calorimeter terdiri daripada bikar silinder bersalut timah, varnis, yang dipegang oleh tripod dan secara dalaman ditamatkan dengan corong. Di dalamnya, satu lagi kaca diletakkan, serupa dengan yang terdahulu, dengan tiub yang melalui ruang luar dan yang disediakan dengan kunci. Di dalam gelas kedua ialah grid.
Dalam grid ini diletakkan makhluk atau objek yang haba tertentu dikehendaki ditentukan. Ais diletakkan di dalam kapal konsentrik, sama seperti dalam bakul.
Haba yang dihasilkan oleh badan diserap oleh ais, menyebabkan peleburannya. Dan produk air cair dari lebur ais dikumpulkan, membuka kunci kaca dalam.
Dan akhirnya, menimbang air, jisim ais lebur itu diketahui.
Bahagian
Calorimeter yang paling biasa digunakan dalam makmal pengajaran kimia adalah calorimeter cawan kopi yang dipanggil. Calorimeter ini terdiri daripada bikar, atau sebaliknya, bekas bahan anime yang mempunyai sifat penebat tertentu. Di dalam bekas ini larutan akueus diletakkan dengan badan yang akan menghasilkan atau menyerap haba.
Di bahagian atas bekas, penutup bahan penebat dengan dua lubang diletakkan. Dalam satu termometer diperkenalkan untuk mengukur perubahan suhu, dan pada pengaduk yang lain, sebaik-baiknya bahan kaca, yang melaksanakan fungsi mengalihkan kandungan larutan berair.
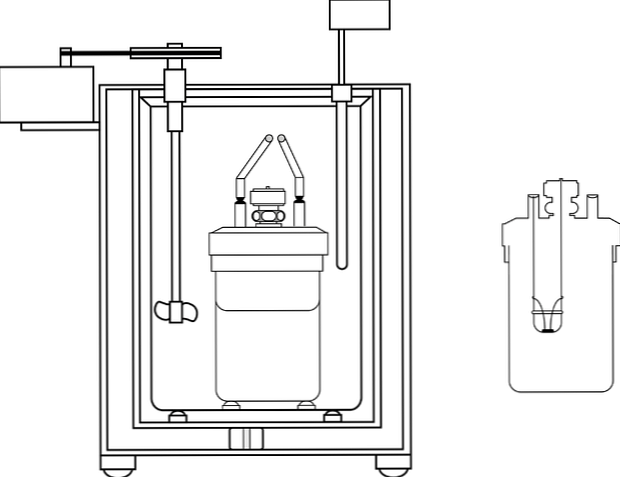
Imej menunjukkan bahagian-bahagian pam kalorimetri; Walau bagaimanapun, ia dapat diperhatikan bahawa ia mempunyai termometer dan agitator, unsur biasa dalam beberapa calorimeters.
Jenis dan ciri-ciri mereka
Cawan kopi
Ia adalah satu yang digunakan dalam penentuan haba yang dikeluarkan oleh reaksi eksotermik, dan haba diserap dalam reaksi endotermik.
Di samping itu, ia boleh digunakan untuk menentukan haba tertentu badan; iaitu jumlah haba yang gram bahan perlu diserap untuk menaikkan suhunya dengan satu darjah Celsius. .
Pam calorimetrik
Ia adalah peranti di mana jumlah haba yang dilepaskan atau diserap dalam reaksi yang berlaku pada isipadu malar diukur.
Reaksi berlaku di dalam kapal keluli yang kuat (pam), yang direndam dalam jumlah besar air. Ini menjadikan perubahan suhu air kecil. Oleh itu, diandaikan bahawa perubahan yang berkaitan dengan reaksi diukur pada suhu dan isipadu malar.
Di atas menunjukkan bahawa tiada kerja dilakukan apabila tindak balas dilakukan dalam pam kalori.
Reaksi bermula dengan membekalkan elektrik melalui kabel yang disambungkan ke pam.
Kaloriim adiabatik
Ia dicirikan dengan mempunyai struktur penebat dipanggil perisai. Perisai terletak di sekitar sel di mana perubahan haba dan suhu berlaku. Ia juga dihubungkan dengan sistem elektronik yang mengekalkan suhunya sangat dekat dengan sel tersebut, untuk mengelakkan pemindahan haba.
Dalam calorimeter adiabatik, perbezaan suhu di antara kalorimeter dan persekitarannya diminimumkan; serta meminimumkan pekali pemindahan haba dan masa untuk pertukaran haba.
Bahagiannya terdiri daripada yang berikut:
-Sel (atau bekas), disatukan ke dalam sistem penebat yang mana ia cuba untuk mengelakkan kehilangan haba.
-Termometer, untuk mengukur perubahan suhu.
-Pemanas, disambungkan kepada sumber voltan elektrik yang dikawal.
-Dan perisai, sudah disebutkan.
Dalam calorimeter jenis ini, sifat seperti entropi, suhu Debye dan ketumpatan keadaan elektronik boleh ditentukan.
Kalori isoperibolic
Ini adalah peranti di mana sel tindak balas dan pam dibakar dalam struktur yang dipanggil jaket. Dalam kes ini, jaket yang dipanggil terdiri daripada air, disimpan pada suhu malar.
Suhu sel dan pam meningkat apabila haba dikeluarkan semasa proses pembakaran; tetapi suhu jaket air dikekalkan pada suhu tetap.
Mikropemproses mengawal suhu sel dan jaket, menjadikan pembetulan yang diperlukan haba kebocoran yang berpunca dari perbezaan antara kedua-dua suhu.
Pembetulan ini diteruskan secara berterusan, dan dengan pembetulan terakhir, berdasarkan pengukuran sebelum dan selepas ujian.
Calorimeter aliran
Dibangunkan oleh Caliendar, ia mempunyai peranti untuk memindahkan gas dalam bekas pada kelajuan yang tetap. Apabila menambah haba, peningkatan suhu dalam bendalir diukur.
Kalorimeter aliran dicirikan oleh:
- Pengukuran yang tepat mengenai kadar aliran malar.
- Pengukuran tepat jumlah haba yang dimasukkan ke dalam bendalir melalui pemanas.
- Pengukuran yang tepat mengenai kenaikan suhu dalam gas yang disebabkan oleh input tenaga
- Reka bentuk untuk mengukur kapasiti gas di bawah tekanan.
Calorimeter untuk kalori pengimbasan berbeza
Ia dicirikan dengan mempunyai dua bekas: dalam satu sampel yang akan dipelajari diletakkan, sementara yang lain disimpan kosong atau bahan rujukan digunakan.
Dua kapal itu dipanaskan pada kelajuan tenaga yang berterusan, dengan menggunakan dua pemanas bebas. Apabila pemanasan kedua-dua kontena bermula, komputer akan menggambarkan perbezaan aliran haba pemanas terhadap suhu, dengan itu dapat menentukan aliran haba.
Di samping itu, variasi suhu sebagai fungsi masa boleh ditentukan; dan akhirnya, keupayaan kalori.
Permohonan
Dalam fizikokimia
-Calorimetri asas, jenis cawan kopi, membolehkan untuk mengukur jumlah haba yang dibebaskan atau diserap oleh badan. Mereka boleh menentukan sama ada tindak balas adalah eksotermik atau endotermik. Di samping itu, haba tertentu badan boleh ditentukan.
-Dengan calorimeter adiabatik ia mungkin untuk menentukan entropi proses kimia dan ketumpatan elektronik keadaan.
Dalam sistem biologi
-Microcalorimeters digunakan untuk mengkaji sistem biologi yang merangkumi interaksi antara molekul, serta perubahan konformasi molekul yang berlaku; sebagai contoh, dalam pembukaan molekul. Baris ini mengandungi kedua-dua pengesanan pembezaan dan titisan isoterma.
-Mikrosalorimeter digunakan dalam pembangunan ubat-ubatan molekul kecil, bioterapeutik dan vaksin.
Calorimeter pam oksigen dan kuasa kalori
Pembakaran pelbagai bahan berlaku dalam calorimeter pam oksigen, dan kuasa kalorinya dapat ditentukan. Antara bahan yang dikaji melalui penggunaan calorimeter ini ialah: arang batu dan kok; minyak yang boleh dimakan, baik berat dan ringan; petrol dan semua bahan api motor.
Serta jenis bahan api untuk reaktor pesawat; sisa bahan api dan pelupusan sisa; produk makanan dan suplemen untuk pemakanan manusia; tanaman makanan ternakan dan suplemen makanan haiwan; bahan binaan; roket dan bahan api propelan.
Begitu juga, kuasa kalori telah ditentukan oleh kalorimetri dalam kajian termodinamik bahan mudah terbakar; dalam kajian keseimbangan tenaga dalam ekologi; dalam bahan letupan dan serbuk haba dan dalam pengajaran kaedah termodinamik asas.
Rujukan
- Whitten, Davis, Peck & Stanley. Kimia (Ed ed.). Pembelajaran CENGAGE.
- González J., Cortés L. & Sánchez A. (s.f.). Kaloriim Adiabatik dan aplikasinya. Pulih daripada: cenam.mx
- Wikipedia. (2018). Calorimeter. Diperolehi daripada: en.wikipedia.org
- Helmenstine, Anne Marie, Ph.D. (22 Jun, 2018). Definisi Calorimeter dalam Kimia. Diperolehi daripada: thoughtco.com
- Gillespie, Claire. (11 April 2018). Bagaimana Calorimeter berfungsi? Saintifik. Diperolehi daripada: sciencing.com


