Kalsium fosfat (Ca3 (PO4) 2) struktur, sifat, pembentukan dan kegunaan
The kalsium fosfat adalah garam anorganik dan tersier yang formula kimianya ialah Ca3(PO4)2. Formula menyatakan bahawa komposisi garam ini adalah 3: 2 untuk kalsium dan fosfat. Ini dapat dilihat secara langsung pada imej yang lebih rendah, di mana Ca cation ditunjukkan2+ dan anion PO43-. Untuk setiap tiga Ca2+ Terdapat dua PO43- berinteraksi dengan mereka.
Sebaliknya, kalsium fosfat merujuk kepada satu siri garam yang berbeza bergantung pada nisbah Ca / P, serta tahap penghidratan dan pH. Malah, terdapat banyak jenis kalsium fosfat yang wujud dan boleh disintesis. Walau bagaimanapun, mengikut nomenklaturnya secara literal, kalsium fosfat hanya merujuk kepada trikalcium, yang disebutkan di atas.

Semua kalsium fosfat, termasuk Ca3(PO4)2, Mereka adalah putih pepejal dengan nada kelabu yang sedikit. Mereka boleh berbutir, halus, kristal, dan mempunyai saiz zarah yang terdapat di sekeliling mikrometer; dan bahkan, nanopartikel fosfat ini telah disediakan, dengan bahan biokompatibel untuk tulang direka.
Keabsahan ini disebabkan oleh fakta bahawa garam ini terdapat di gigi dan, dalam jangka pendek, dalam tisu tulang mamalia. Sebagai contoh, hidroksiapatit adalah kalsium fosfat kristal, yang seterusnya berinteraksi dengan fasa amorf daripada garam yang sama.
Ini bermakna fosfat kalsium amorfus dan kristal wujud. Atas sebab ini, kepelbagaian dan pelbagai pilihan tidak menghairankan apabila bahan sintesis berdasarkan kalsium fosfat; bahan-bahan yang sifatnya penyelidik lebih berminat setiap hari di seluruh dunia untuk menumpukan pada pemulihan tulang.
Indeks
- 1 Struktur kalsium fosfat
- 1.1 Kalsium fosfat amorf
- 1.2 Selebihnya keluarga
- 2 Sifat fizikal dan kimia
- 2.1 Nama
- 2.2 Berat molekul
- 2.3 Penerangan fizikal
- 2.4 Rasa
- 2.5 Takat lebur
- 2.6 Keterlarutan
- 2.7 Ketumpatan
- 2.8 Indeks refraktif
- 2.9 Latihan entalpi standard
- 2.10 Suhu penyimpanan
- 2.11 pH
- 3 Latihan
- 3.1 Kalsium nitrat dan ammonium hidrogen fosfat
- 3.2 Kalsium hidroksida dan asid fosforik
- 4 Kegunaan
- 4.1 Dalam tisu tulang
- 4.2 Semen Biokeramik
- 4.3 Doktor
- 4.4 Lain-lain
- 5 Rujukan
Struktur kalsium fosfat
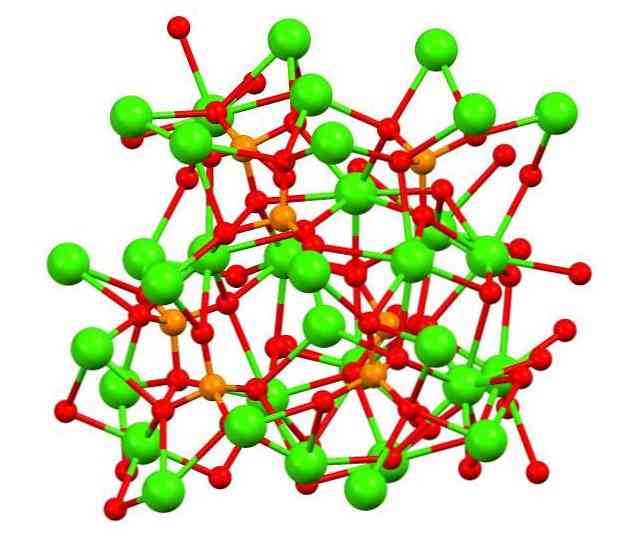
Imej atas menunjukkan struktur fosfat calico tribasik dalam mineral whitlockite aneh, yang mungkin mengandungi magnesium dan besi sebagai kekotoran.
Walaupun pada pandangan pertama ia kelihatannya rumit, adalah perlu untuk menjelaskan bahawa model itu menganggap interaksi kovalen antara atom oksigen fosfat dan pusat logam kalsium.
Oleh cara perwakilan adalah sah, bagaimanapun, interaksi itu adalah elektrostatik; iaitu, kation Ca2+ tertarik kepada anion PO43- (Ca2+- O-PO33-). Dengan ini, difahami mengapa dalam kalsium imej (sfera hijau) dikelilingi oleh atom oksigen yang dikenakan negatif (sfera merah).
Apabila terdapat begitu banyak ion, ia tidak meninggalkan susunan simetri atau corak yang boleh dilihat. The Ca3(PO4)2 Mengamalkan suhu rendah (T<1000°C) una celda unitaria correspondiente a un sistema cristalino romboédrico; a este polimorfo se le conoce con el nombre de β-Ca3(PO4)2 (β-TCP, untuk akronim dalam bahasa Inggeris).
Pada suhu tinggi, sebaliknya, ia berubah menjadi polimorf α-Ca3(PO4)2 (α-TCP), yang sel unitnya sepadan dengan sistem kristal monoklinik. Pada suhu yang lebih tinggi, polimorf α'-Ca juga boleh dibentuk3(PO4)2, yang terdiri daripada struktur kristal heksagon.
Kalsium fosfat amorfus
Struktur kristal telah disebutkan untuk kalsium fosfat, yang diharapkan dari garam. Walau bagaimanapun, ia mampu mempamerkan struktur tidak teratur dan tidak simetri, yang dikaitkan dengan lebih banyak jenis "kalsium fosfat kaca" daripada kristal dalam erti kata ketat definisi.
Apabila ini berlaku, dikatakan bahawa kalsium fosfat mempunyai struktur amorf (ACP, kalsium fosfat amorf). Beberapa penulis menunjuk struktur jenis ini yang bertanggungjawab terhadap sifat biologi Ca3(PO4)2 dalam tisu tulang, pembaikan dan biomimetisasi mungkin.
Melalui penjelasan strukturnya oleh resonans magnetik nuklear (NMR), kehadiran ion OH telah dijumpai- dan HPO42- di ACP. Ion-ion ini dibentuk oleh hidrolisis salah satu fosfat:
PO43- + H2O <=> HPO42- + OH-
Akibatnya, struktur sebenar ACP menjadi lebih rumit, yang komposisinya ionnya diwakili oleh formula: Ca9(PO4)6-x(HPO4)x(OH)x. The 'x' menunjukkan tahap penghidratan, kerana jika x = 1, maka formula akan seperti: Ca9(PO4)5(HPO4) (OH).
Struktur yang berbeza yang mungkin PCA bergantung pada nisbah molar Ca / P; iaitu jumlah relatif kalsium dan fosfat, yang mengubah semua komposisi yang dihasilkan.
Selebihnya keluarga
Kalsium fosfat sebenarnya adalah keluarga sebatian tak organik, yang boleh berinteraksi dengan matriks organik.
Fosfat lain diperoleh dengan "hanya" dengan mengubah anion yang mengiringi kalsium (PO43-, HPO42-, H2PO4-, OH-), serta jenis kekotoran dalam pepejal. Oleh itu, sehingga sebelas kalsium fosfat atau lebih, masing-masing dengan struktur dan sifatnya sendiri, boleh berasal secara semula jadi atau buatan..
Berikut adalah beberapa fosfat dan struktur dan formula kimia masing-masing:
-Hidrogen kalsium fosfat dihidrat, CaHPO4∙ 2H2O: monoklinik.
-Kalsium dihydrogen fosfat monohidrat, Ca (H)2PO4)2∙ H2O: triklinik.
-Fosfat diacid tanpa asid, Ca (H)2PO4)2: triklinik.
-Ocalcium hydrogen fosfat (OCP), Ca8H2(PO4)6: triklinik Ia adalah prekursor dalam sintesis hydroxyapatite.
-Hydroxyapatite, Ca5(PO4)3OH: hexagonal.
Sifat fizikal dan kimia
Nama-nama
-Kalsium fosfat
-Trikalcium fosfat
-Trikalcium diphosphate
Berat molekul
310.74 g / mol.
Penerangan fizikal
Ia adalah pepejal putih yang tidak berbau.
Rasa
Tidak sempurna.
Titik lebur
1670 ºK (1391ºC).
Kelarutan
-Praktikal tidak larut dalam air.
-Tidak larut dalam etanol.
-Larut dalam asid hidroklorik cair dan asid nitrik.
Ketumpatan
3.14 g / cm3.
Indeks refraktif
1,629
Latihan entalpi standard
4126 kcal / mol.
Suhu penyimpanan
2-8ºC.
pH
6-8 dalam penggantungan akueus 50 g / L kalsium fosfat.
Latihan
Kalsium nitrat dan hidrogen ammonium fosfat
Terdapat banyak kaedah untuk menghasilkan atau membentuk kalsium fosfat. Salah satunya terdiri daripada campuran dua garam, Ca (NO)3)2∙ 4H2O, dan (NH4)2HPO4, sebelum ini dibubarkan dalam alkohol dan air mutlak. Satu garam menyediakan kalsium, dan fosfat yang lain.
Dari campuran ini, ACP akan merangsang, yang kemudiannya akan dipanaskan dalam ketuhar pada 800 ° C dan selama 2 jam. Sebagai hasil dari prosedur ini, β-Ca diperolehi3(PO4)2. Dengan berhati-hati mengawal suhu, gangguan dan masa kenalan, pembentukan nanocrystal boleh berlaku.
Untuk membentuk polimorf α-Ca3(PO4)2 perlu mengeringkan fosfat di atas 1000 ° C. Pemanasan ini dijalankan dengan kehadiran ion logam lain, yang menstabilkan polimorf ini dengan secukupnya untuk digunakan pada suhu bilik; iaitu, ia kekal dalam keadaan meta stabil.
Kalsium hidroksida dan asid fosforik
Kalsium fosfat juga boleh dibentuk dengan mencampurkan larutan kalsium hidroksida dan asid fosforik, dengan peneutralan berasid berasaskan. Selepas setengah hari masak dalam arak ibu, dan penapisannya yang betul, membasuh, mengeringkan dan mengencang, serbuk berbutir fosfat amorf diperoleh, ACP.
Ini produk reaksi ACP suhu tinggi, berubah mengikut persamaan kimia berikut:
2Ca9(HPO4) (PO4)5(OH) => 2Ca9(P.2O7)0.5(PO4)5(OH) + H2O (di T = 446.60 ° C)
2Ca9(P.2O7)0.5(PO4)5(OH) => 3Ca3(PO4)2 + 0.5H2O (di T = 748.56 ° C)
Dengan cara ini, β-Ca diperolehi3(PO4)2, polimorf yang paling biasa dan stabil.
Kegunaan
Dalam tisu tulang
The Ca3(PO4)2 Ia adalah konstituen utama abu tulang. Ia adalah komponen pemindahan tulang pengganti, ini dijelaskan oleh persamaan kimianya dengan mineral yang terdapat pada tulang.
Biomaterial kalsium fosfat digunakan untuk membetulkan kecacatan tulang dan dalam pelapisan prostesis titanium logam. Kalsium fosfat didepositkan kepada mereka, mengasingkannya dari alam sekitar dan memperlahankan proses kakisan titanium.
Kalsium fosfat, termasuk Ca3(PO4)2, Ia digunakan untuk penghasilan bahan seramik. Bahan-bahan ini bersifat biokompatibel, dan kini digunakan untuk memulihkan kehilangan tulang alveolar, yang disebabkan oleh penyakit periodontal, jangkitan endodontik dan keadaan lain..
Walau bagaimanapun, ia hanya perlu digunakan untuk mempercepat pembaikan tulang periapikal, di kawasan yang tidak terdapat jangkitan bakteria kronik.
Kalsium fosfat boleh digunakan untuk membaiki kecacatan tulang, apabila tidak mungkin menggunakan gores tulang autogenous. Ia boleh digunakan sendiri atau digabungkan dengan polimer biodegradable dan resorbable, seperti asid polyglycolic.
Semen bioceramic
Semen kalsium fosfat (CPC) adalah satu lagi biokeramik yang digunakan dalam pembaikan tisu tulang. Ia dibuat dengan mencampurkan serbuk pelbagai jenis kalsium fosfat dengan air, membentuk pes. Pes paste boleh disuntik atau diselaraskan kepada cacat tulang atau rongga.
Semen dibentuk, secara beransur-ansur dikombinasikan dan diganti dengan tulang yang baru terbentuk.
Doktor
-The Ca3(PO4)2 Ia adalah garam asas, jadi ia digunakan sebagai antacid untuk meneutralkan lebihan asid perut dan meningkatkan pH. Dalam ubat gigi, ia menyediakan sumber kalsium dan fosfat untuk memudahkan proses remineralisasi gigi dan hemostasis tulang.
-Ia juga digunakan sebagai suplemen pemakanan, walaupun cara paling murah untuk menggantikan kalsium adalah melalui penggunaan karbonat dan sitratnya..
-Kalsium fosfat boleh digunakan dalam rawatan tetany, hypocalcemia laten dan terapi penyelenggaraan. Di samping itu, ia berguna dalam suplemen kalsium semasa mengandung dan menyusu.
-Ia digunakan dalam rawatan pencemaran dengan radio isotop radioaktif (Ra-226) dan strontium (Sr-90). Kalsium fosfat menyekat penyerapan isotop radioaktif dalam saluran pencernaan, dengan itu mengehadkan kerosakan yang disebabkan oleh mereka.
Lain-lain
-Kalsium fosfat digunakan sebagai makanan untuk burung. Di samping itu, ia digunakan dalam pasta gigi untuk mengawal tartar.
-Ia digunakan sebagai ejen anti-caking, sebagai contoh untuk mengelakkan garam meja daripada dipadatkan.
-Ia berfungsi sebagai agen peluntur untuk tepung. Walaupun, dalam babi babi menghalang pewaran yang tidak diingini dan memperbaiki keadaan menggoreng.
Rujukan
- Tung M.S. (1998) Kalsium fosfat: Struktur, Komposisi, Kelarutan, dan Kestabilan. Dalam: Amjad Z. (eds) Kalsium Phosphates dalam Sistem Biologi dan Perindustrian. Springer, Boston, MA.
- Langlang Liu, Yanzeng Wu, Chao Xu, Suchun Yu, Xiaopei Wu, dan Honglian Dai. (2018). "Sintesis, Pencirian Nano-β-Tricalcium Phosphate dan Inhibisi pada Sel Carcinoma Hepatosellular," Journal of Nanomaterials, vol. 2018, ID Artikel 7083416, 7 halaman, 2018.
- Menggabungkan, Kristus dan Rey, Kristian. (2010). Fosfat kalsium amorf: sintesis, sifat dan kegunaan dalam biomaterial. Acta Biomaterialia, vol. 6 (n ° 9). pp. 3362-3378. ISSN 1742-7061
- Wikipedia. (2019). Trikalcium fosfat. Diperolehi daripada: en.wikipedia.org
- Abida et al. (2017). Trikalcium fosfat serbuk: Penyediaan, pencirian dan pemadatan kebolehan. Jurnal Pertanian Kimia 2017, 6 (3), 71-76.
- PubChem. (2019). Kalsium fosfat. Diperolehi daripada: pubchem.ncbi.nlm.nih.gov
- Elsevier (2019). Kalsium fosfat. Sains Terus. Diperolehi daripada: sciencedirect.com


