Volume Atom Bagaimana Ia Berbeza dalam Jadual Berkala dan Contoh
The jumlah atom adalah nilai relatif yang menunjukkan hubungan antara jisim molar unsur dan ketumpatannya. Oleh itu, jumlah ini bergantung kepada ketumpatan elemen, dan ketumpatannya bergantung pada fasa seterusnya dan bagaimana atom disusun dalam keadaan ini.
Oleh itu, isipadu atom untuk unsur Z tidak sama dalam fasa lain yang berbeza dari yang ditunjukkan pada suhu bilik (cecair, pepejal atau gas), atau apabila ia adalah sebahagian daripada sebatian tertentu. Oleh itu, isipadu atom Z dalam sebatian ZA adalah berbeza daripada Z dalam sebatian ZB.

Mengapa? Untuk memahaminya, adalah perlu untuk membandingkan atom dengan, contohnya, guli. Kelereng, seperti imej kebiruan dari imej yang unggul, telah menentukan batas materialnya dengan baik, yang diperhatikan berkat permukaan yang cemerlang. Sebaliknya, sempadan atom adalah meresap, walaupun ia boleh dianggap jauh dari sfera.
Oleh itu, apa yang menentukan titik di luar sempadan atom adalah kebarangkalian nol untuk mencari elektron, dan titik ini mungkin lebih jauh atau lebih dekat dengan nukleus bergantung kepada berapa banyak atom jiran berinteraksi di sekitar atom yang dipertimbangkan.
Indeks
- 1 Kuantiti dan jejari atom
- 2 formula tambahan
- 3 Bagaimanakah jumlah atom berbeza dalam jadual berkala??
- 3.1 Logam peralihan isipadu atom
- 4 Contoh
- 4.1 Contoh 1
- 4.2 Contoh 2
- 5 Rujukan
Jumlah dan radius atom
Dengan berinteraksi dua atom H dalam molekul H2, kedudukan nukleus mereka ditakrifkan serta jarak di antara mereka (jarak internuclear). Sekiranya kedua-dua atom sfera, jejari adalah jarak antara nukleus dan sempadan tersebar:
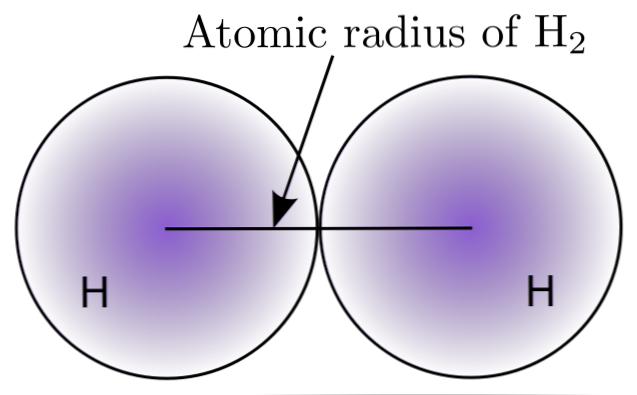
Dalam imej atas dapat dilihat bagaimana kebarangkalian mencari elektron berkurang apabila ia bergerak dari nukleus. Membahagikan jarak internuclear antara dua, radius atom diperolehi. Seterusnya, dengan menganggap geometri sfera untuk atom, kami menggunakan formula untuk mengira isipadu sfera:
V = (4/3) (Pi) r3
Dalam ungkapan ini r ialah jejari atom yang ditetapkan untuk molekul H2. Nilai V yang dikira oleh kaedah tidak tepat ini boleh berubah jika, sebagai contoh, ia dianggap H2 dalam keadaan cecair atau logam. Walau bagaimanapun, kaedah ini sangat tidak tepat kerana bentuk atom jauh dari sfera ideal dalam interaksi mereka.
Untuk menentukan jumlah atom dalam pepejal, banyak pembolehubah mengenai perkiraan diambil kira, dan diperolehi oleh kajian difraksi sinar-X..
Formula tambahan
Jisim molar mengekspresikan jumlah bahan yang mempunyai satu mole atom unsur kimia.
Unitnya adalah g / mol. Sebaliknya, ketumpatan adalah isipadu yang menduduki satu gram unsur: g / mL. Kerana unit isipadu atom adalah mL / mol, anda perlu bermain dengan pemboleh ubah untuk mencapai unit yang dikehendaki:
(g / mol) (mL / g) = mL / mol
Atau apa yang sama:
(Molar massa) (1 / D) = V
(Molar massa / D) = V
Oleh itu, isipadu satu mole atom unsur dapat dikira dengan mudah; manakala dengan rumus isipadu sfera isipadu atom individu dikira. Untuk mencapai nilai ini dari yang pertama, penukaran diperlukan melalui nombor Avogadro (6.02 · 10).-23).
Bagaimanakah jumlah atom berbeza dalam jadual berkala??
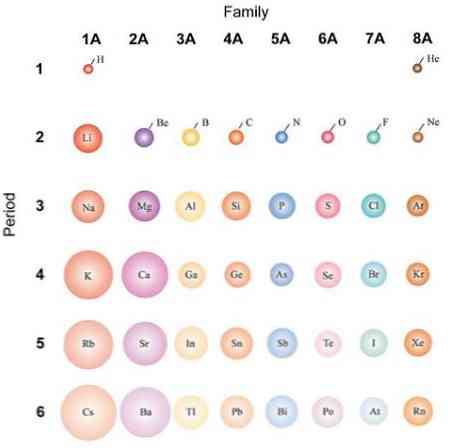
Jika atom dianggap sfera, maka variasi mereka akan sama seperti diamati dalam radius atom. Dalam imej atas, yang menunjukkan unsur-unsur wakil, ia digambarkan bahawa dari kanan ke kiri kerdil atom; sebaliknya, dari atas ke bawah ini menjadi lebih besar.
Ini kerana pada masa yang sama nukleus menggabungkan proton ketika bergerak ke kanan. Proton ini menghasilkan daya yang menarik pada elektron luaran, yang merasakan caj nuklear yang berkesan Zef, kurang daripada caj nuklear sebenar Z.
Elektron lapisan dalaman mengusir lapisan luar, mengurangkan kesan nukleus ke atas; Ini dikenali sebagai kesan skrin. Dalam tempoh yang sama, kesan skrin tidak dapat mengatasi peningkatan bilangan proton, jadi elektron di lapisan dalam tidak menghalang penguncupan atom.
Walau bagaimanapun, dengan turun ke dalam kumpulan, tahap tenaga baru diaktifkan, yang membolehkan elektron mengorbit jauh dari nukleus. Juga, bilangan elektron dalam lapisan dalaman meningkat, yang kesan perisai mula berkurang jika nukleus menambah proton lagi.
Atas sebab-sebab ini dapat dilihat bahawa kumpulan 1A mempunyai atom yang paling besar, tidak seperti atom-atom kecil dari kumpulan 8A (atau 18), gas-gas mulia.
Jumlah atom peralihan atom
Atom atom peralihan menggabungkan elektron ke orbital dalaman d. Peningkatan kesan skrin dan, serta caj nuklear sebenar Z, dibatalkan hampir sama, supaya atom mereka mengekalkan saiz yang serupa dalam tempoh yang sama.
Dalam erti kata lain: dalam satu tempoh, logam peralihan mempamerkan jumlah atom yang serupa. Walau bagaimanapun, perbezaan kecil ini sangat ketara apabila menentukan kristal logam (seolah-olah mereka adalah logam guli).
Contohnya
Dua formula matematik tersedia untuk mengira isipadu atom unsur, masing-masing dengan contohnya yang sepadan.
Contoh 1
Memandangkan radius atom hidrogen -37 malam (1 picometer = 10-12m) - dan sesium -265 pm-, hitung isipadu atomnya.
Dengan menggunakan formula isipadu sfera, kami mempunyai:
VH= (4/3) (3.14) (37 malam)3= 212.07 petang3
VCs= (4/3) (3.14) (265 malam)3= 77912297,67 petang3
Walau bagaimanapun, jumlah yang dinyatakan dalam pyrometers adalah terlalu tinggi, jadi ia berubah menjadi unit angstrom, mendarabkannya dengan faktor penukaran (1 Å / 100pm)3:
(212.07 petang3) (1 pagi / 100 malam)3= 2.1207 × 10-4 Å3
(77912297,67 petang3) (1 pagi / 100 malam)3= 77,912 Å3
Oleh itu, perbezaan saiz antara atom kecil H dan atom besar Cs kekal jelas secara berangka. Perlu diingat bahawa pengiraan ini hanya perkiraan di bawah tuntutan bahawa atom adalah sfera yang sama sekali, yang mengembara di muka realiti.
Contoh 2

Ketumpatan emas murni ialah 19.32 g / mL dan jisim molarnya ialah 196.97 g / mol. Memohon formula M / D untuk mengira isipadu satu tahi atom emas mempunyai berikut:
VAu= (196.97 g / mol) / (19.32 g / mL) = 10.19 mL / mol
Iaitu, 1 mole atom emas menempati 10.19 mL, tetapi jumlah kuantiti atom emas yang tertentu? Dan bagaimana untuk menyatakannya dalam unit pm3? Untuk ini hanya semata-mata menerapkan faktor penukaran berikut:
(10.19 mL / mol) · (mol / 6.02 · 10)-23 atom) · (1 m / 100 cm)3· (1 petang / 10-12m)3= 16,92 · 106 petang3
Di sisi lain, jejari atom emas ialah 166 malam. Jika anda membandingkan kedua-dua jilid - yang diperolehi dengan kaedah sebelumnya dan yang dikira dengan rumus isipadu sfera - anda akan mendapati bahawa mereka tidak mempunyai nilai yang sama:
VAu= (4/3) (3.14) (166 malam)3= 19.15 · 106 petang3
Mana satu daripada yang paling dekat dengan nilai yang diterima? Yang paling dekat dengan keputusan percubaan yang diperolehi oleh penyelarasan sinar-X struktur kristal emas.
Rujukan
- Helmenstine, Anne Marie, Ph.D. (09 Disember 2017). Definisi Kelantangan Atom. Diperoleh pada 6 Jun, 2018, dari: thoughtco.com
- Mayfair, Andrew. (13 Mac, 2018). Bagaimana Menghitung Jilid Atom. Saintifik. Diperoleh pada 6 Jun, 2018, dari: sciencing.com
- Wiki Kids Ltd. (2018). Lothar Meyer Curve Volume Atom. Diambil pada 6 Jun 2018, dari: wonderwhizkids.com
- Lumen Trend Berkala: Radius Atom. Diperoleh pada 6 Jun 2018, dari: courses.lumenlearning.com
- Camilo J. Derpich. Ketumpatan volum dan atom. Diperoleh pada 6 Jun 2018, dari: es-puraquimica.weebly.com
- Whitten, Davis, Peck & Stanley. Kimia (Ed ed.). CENGAGE Learning, p 222-224.
- Yayasan CK-12. (22 Februari 2010). Saiz atom perbandingan. [Rajah] Diperoleh pada 6 Jun 2018, dari: commons.wikimedia.org
- Yayasan CK-12. (22 Februari 2010). Radius atom H2. [Rajah] Diperoleh pada 6 Jun 2018, dari: commons.wikimedia.org


