Struktur, Properties dan Kegunaan Kalsium Oksida (CaO)
The kalsium oksida (CaO) adalah sebatian anorganik yang mengandungi kalsium dan oksigen dalam bentuk ionik (tidak boleh dikelirukan dengan kalsium peroksida, CaO2). Ia dikenali di seluruh dunia sebagai kapur, satu perkataan yang menunjuk sebatian anorganik yang mengandungi karbonat, kalsium oksida dan hidroksida, serta logam lain seperti silikon, aluminium dan besi..
Oksida ini (atau kapur) juga dirujuk secara colloquially sebagai limau kapsul atau slaked, bergantung kepada sama ada ia terhidrasi atau tidak. Lime adalah kalsium oksida, manakala kapur yang digoreng adalah hidroksida. Sebaliknya, batu kapur (batu kapur atau kapur keras) sebenarnya merupakan batu sedimen yang terdiri terutamanya dari kalsium karbonat (CaCO3).

Ia adalah salah satu sumber kalsium semula jadi terbesar dan merupakan bahan mentah untuk pengeluaran kalsium oksida. Bagaimanakah oksida ini dihasilkan? Karbonat mudah terdedah kepada penguraian terma; Pemanasan kalsium karbonat pada suhu di atas 825 ° C, yang membawa kepada pembentukan kapur dan karbon dioksida.
Kenyataan di atas boleh dihuraikan seperti berikut: CaCO3(s) → CaO (s) + CO2(g) Kerana kerak Bumi kaya dengan batu kapur dan calcite, dan lautan dan pantai adalah kerang yang banyak (bahan-bahan mentah untuk pengeluaran kalsium oksida), kalsium oksida reagen agak murah.
Indeks
- 1 Formula
- 2 Struktur
- 3 Hartanah
- 3.1 Keterlarutan
- 4 Kegunaan
- 4.1 Sebagai mortar
- 4.2 Dalam pengeluaran gelas
- 4.3 Dalam perlombongan
- 4.4 Sebagai penghilang silikat
- 5 nanopartikel kalsium oksida
- 6 Rujukan
Formula
Rumus kimia kalsium oksida adalah CaO, di mana kalsium seperti ion asid (penerima elektron) Ca2+, dan oksigen sebagai ion asas (penderma elektron) ATAU2--.
Mengapa kalsium mempunyai caj +2? Kerana kalsium tergolong dalam kumpulan 2 dari jadual berkala (Mr. Becambara), dan hanya mempunyai dua elektron valensi yang tersedia untuk pembentukan ikatan, yang menghasilkan atom oksigen.
Struktur
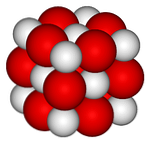
Dalam imej atas, struktur kristal (jenis permata-garam) untuk kalsium oksida diwakili. Sfera merah besar sesuai dengan ion Ca2+ dan sfera putih ke ion O2-.
Dalam susunan kristal padu ini setiap ion Ca2+ dikelilingi oleh enam ion O2-, tersekat di lubang oktahedral yang ditinggalkan oleh ion besar di antara mereka.
Struktur ini meluahkan watak ionik maksimum oksida, walaupun perbezaan besar jejari (sfera merah adalah lebih besar daripada putih) memberi tenaga kristal kekisi yang lebih lemah jika dibandingkan dengan MgO.
Hartanah
Secara fizikal, ia adalah pepejal putih kristal, tidak berbau dan dengan interaksi elektrostatik yang kuat, yang bertanggungjawab untuk titik leburnya yang tinggi (2572 ° C) dan mendidih (2850 ° C). Di samping itu, ia mempunyai berat molekul 55,958 g / mol dan harta yang menarik menjadi termoluminesin.
Ini bermakna sekeping kalsium oksida yang terdedah kepada api boleh bersinar dengan cahaya putih yang kuat, yang dikenali dalam bahasa Inggeris dengan nama perhatian, atau dalam bahasa Sepanyol, cahaya kalsium. Ion Ca2+, bersentuhan dengan api, mereka menyebabkan api kemerah-merahan, seperti yang ditunjukkan dalam imej berikut.

Kelarutan
CaO ialah oksida asas yang mempunyai pertalian yang kuat untuk air, sedemikian rupa sehingga menyerap kelembapan (adalah pepejal hygroscopic) dan bertindak balas dengan segera untuk menghasilkan kapur mati atau kalsium hidroksida:
CaO (s) + H2O (l) => Ca (OH)2(s)
Tindak balas ini adalah exothermic (melepaskan haba) disebabkan oleh pembentukan pepejal dengan interaksi yang lebih kuat dan kisi kristal yang lebih stabil. Walau bagaimanapun, tindak balas itu boleh diterbalikkan jika Ca (OH) dipanaskan2, dehydrating dan menyalakan limau yang teracung; maka, kapur "dilahirkan semula".
Penyelesaian yang terhasil sangat asas, dan jika ia tepu dengan kalsium oksida ia mencapai pH 12.8.
Begitu juga, ia larut dalam gliserol dan penyelesaian asid dan gula. Oleh kerana ia adalah oksida asas, secara semulajadi ia mempunyai interaksi berkesan dengan oksida asid (SiO2, Al2O3 dan Iman2O3, contohnya) larut dalam fasa cecair daripadanya. Sebaliknya, ia tidak larut dalam alkohol dan pelarut organik.
Kegunaan
CaO mempunyai pelbagai luas kegunaan industri serta dalam sintesis asetilena (CH≡CH), dalam menghapuskan fosfat daripada kumbahan dan tindak balas dengan sulfur dioksida daripada sisa gas.
Penggunaan kalsium oksida lain diterangkan di bawah:
Sebagai mortar
Sekiranya kalsium oksida bercampur dengan pasir (SiO2) dan air, kek dengan pasir dan bereaksi perlahan-lahan dengan air untuk membentuk limau slaked. Sebaliknya, CO2 daripada udara larut dalam air dan bertindak balas dengan garam untuk membentuk kalsium karbonat:
Ca (OH)2(s) + CO2(g) => CaCO3(s) + H2O (l)
The CaCO3 Ia adalah sebatian yang lebih tahan dan lebih keras daripada CaO, menyebabkan mortar (campuran sebelumnya) mengeras dan membetulkan bata, blok atau seramik di antara mereka atau ke permukaan yang dikehendaki.
Dalam pengeluaran gelas
Bahan mentah penting untuk pengeluaran gelas adalah oksida silikon, yang dicampurkan dengan kapur, natrium karbonat (Na2CO3) dan bahan tambahan lain, kemudian dikenakan pemanasan, mengakibatkan pepejal kaca. Padu ini kemudiannya dipanaskan dan ditiup dalam sebarang angka.
Dalam perlombongan
Jeruk kapur menduduki jumlah yang lebih tinggi daripada asid sulfur kerana interaksi ikatan hidrogen (O-H-O). Harta ini digunakan untuk memecahkan batu-batu dari dalam.
Ini dicapai dengan mengisi mereka dengan campuran padat kapur dan air, yang dimeterai untuk memfokuskan haba dan kuasa luas di dalam batuan.
Sebagai remover silikat
CaO bersatu dengan silikat untuk membentuk cecair bersatu, yang kemudian diekstraksi dari bahan mentah produk tertentu.
Sebagai contoh, bijih besi adalah bahan mentah untuk pengeluaran besi dan keluli logam. Galian-galian ini mengandungi silikat, yang merupakan kekotoran yang tidak diingini untuk proses tersebut dan dihapuskan dengan kaedah yang digambarkan.
Nanopartikel kalsium oksida
Kalsium oksida boleh disintesis sebagai nanopartikel, berbeza-beza kepekatan kalsium nitrat (Ca (NO3)2) dan natrium hidroksida (NaOH) dalam larutan.
Zarah-zarah ini adalah sfera, asas (serta pepejal skala makro) dan mempunyai banyak kawasan permukaan. Oleh itu, sifat-sifat ini memberi manfaat kepada proses pemangkin. Yang mana? Siasatan sedang menjawab soalan itu.
Kami menggunakan nanopartikel ini untuk mensintesis sebatian organik seperti derivatif diganti piridinas- dalam membangunkan ubat baru untuk melaksanakan transformasi kimia seperti fotosintesis buatan, untuk pembersihan air dari logam berat dan berbahaya, dan sebagai ejen photocatalytic.
Nanopartikel boleh disintesis atas sokongan biologi, seperti daun pepaya dan teh hijau, untuk digunakan sebagai agen antibakteria.
Rujukan
- scifun.org (2018). Lime: kalsium oksida. Diperoleh pada 30 Mac, 2018, dari: scifun.org.
- Wikipedia. (2018). Kalsium oksida. Diambil pada 30 Mac, 2018, dari: en.wikipedia.org
- Ashwini Anantharaman et al. (2016). Sintesis Hijau Nanopartikel Kalsium Oksida dan Aplikasinya. Int. Jurnal Penyelidikan dan Aplikasi Kejuruteraan. ISSN: 2248-9622, Vol. 6, Keluaran 10, (Bahagian -1), ms.27-31.
- J. Safaei-Ghomi et al. (2013). Nanopartikel kalsium oksida catalyzed sintesis multicomponent satu langkah pyridines sangat diganti dalam medium etanol berair Scientia Iranica, Transaksi C: Kimia dan Kejuruteraan Kimia 20 549-554.
- PubChem. (2018). Kalsium oksida. Diambil pada 30 Mac, 2018, dari: pubchem.ncbi.nlm.nih.gov
- Shiver & Atkins. (2008). Kimia anorganik In Unsur kumpulan 2. (edisi keempat, halaman 280). Mc Graw Hill.


