Potensi Iodoate Properties, Struktur, Kegunaan dan Risiko
The kalium iodate atau kalium iodate adalah sebatian anorganik iodin, khususnya garam, yang formula kimianya adalah KIO3. Iodin, unsur kumpulan halogens (F, Cl, Br, I, As), mempunyai garam ini sebagai nombor pengoksidaan +5; kerana ini ia adalah agen pengoksidaan yang kuat. KIO3 memisahkan dalam medium berair untuk mencipta ion K+ dan IO3-.
Ia disintesis dengan bertindak balas terhadap kalium hidroksida dengan asid iodik: HIO3(aq) + KOH (s) => KIO3(aq) + H2O (l) Juga, ia boleh disintesis dengan bertindak balas terhadap molekul molekul dengan potassium hydroxide: 3I2(s) + 6KOH (s) => KIO3(aq) + 5KI (aq) + 3H2O (l).

Indeks
- 1 Sifat fizikal dan kimia
- 1.1 agen pengoksida
- 2 Struktur kimia
- 3 Kegunaan dan penggunaan kalium iodate
- 3.1 Penggunaan terapeutik
- 3.2 Digunakan dalam industri
- 3.3 Penggunaan analitik
- 3.4 Digunakan dalam teknologi laser
- 4 Risiko kesihatan kalium iodate
- 5 Rujukan
Sifat fizikal dan kimia
Ia adalah pepejal putih tanpa bau, dengan kristal halus dan struktur kristal jenis monoklinik. Ia mempunyai kepadatan 3.98 g / mL, berat molekul 214 g / mol dan mempunyai jalur penyerapan dalam spektrum inframerah (IR).
Ia mempunyai titik lebur: 833 ºK (560 ºC), selaras dengan interaksi ionik yang kuat antara K ion+ dan IO3-. Pada suhu yang lebih tinggi, ia mengalami reaksi penguraian haba, melepaskan oksigen molekul dan kalium iodida:
2KIO3(s) => 2KI (s) + 3O2(g)
Di dalam air ia mempunyai kelarutan yang berbeza-beza dari 4.74g / 100mL hingga 0ºC, sehingga 32.3 g / 100mL pada 100ºC, menghasilkan penyelesaian berair tanpa warna. Di samping itu, ia tidak larut dalam asid alkohol dan nitrik, tetapi larut dalam asid sulfurik cair.
Perkaitannya dengan air tidak dapat dijelaskan, yang menjelaskan mengapa ia tidak bersifat hygroscopic dan tidak wujud dalam bentuk garam terhidrasi (KIO)3· H2O).
Ejen pengoksida
Iodate kalium, seperti yang ditunjukkan oleh formula kimianya, mempunyai tiga atom oksigen. Ini adalah unsur elektronegatif yang kuat dan, disebabkan oleh harta ini, ia "membuka" kekurangan elektronik di awan yang mengelilingi iodin.
kekurangan ini, atau input, sebagai kes itu- boleh dikira sebagai jumlah pengoksidaan iodin (± 1, 2, 3, 5, 7), yang merupakan 5 dalam hal garam ini.
Apa maksudnya? Bahawa sebelum spesis yang mampu menghasilkan elektron, iodin akan menerimanya dalam bentuk ioniknya (IO3-) untuk menjadi iodin molekul dan mempunyai nombor pengoksidaan bersamaan dengan 0.
Berikutan penjelasan ini, boleh ditentukan bahawa kalium iodate adalah sebatian pengoksidaan yang bertindak balas dengan kuat dengan mengurangkan agen dalam banyak reaksi redoks; daripada semua ini, satu dikenali sebagai jam iodin.
Jam iodin terdiri daripada proses redoks langkah-langkah yang perlahan dan cepat, di mana langkah cepat ditandai dengan penyelesaian KIO3 dalam asid sulfurik yang mana kanji ditambah. Seterusnya, kanji - sekali dihasilkan dan berlabuh di antara spesies strukturnya I3-- akan mengubah penyelesaian dari warna tanpa warna menjadi biru gelap.
IO3- + 3 HSO3- → Saya- + 3 HSO4-
IO3- + 5 Saya- + 6 H+ → 3 Saya2 + 3 H2O
Saya2 + HSO3- + H2O → 2 I- + HSO4- + 2 H+ (biru gelap kerana kesan kanji)
Struktur kimia
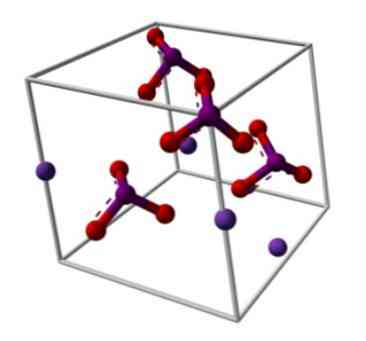
Struktur kimia kalium iodate digambarkan dalam imej atas. Anion IO3- diwakili oleh "tripod" sfera merah dan ungu, manakala K ion+ mereka diwakili oleh sfera ungu.
Tetapi apakah maksud tripod ini? Bentuk geometri betul anion ini sebenarnya piramid trigonal, di mana oksigen membentuk asas segi tiga, dan pasangan itu unshared mata elektron iodin ke atas, berkongsi ruang dan memaksa lipat ke bawah link IO dan dua pautan I = O.
Geometri molekul ini sepadan dengan hibridisasi sp3 atom iodin tengah; Walau bagaimanapun, perspektif lain menunjukkan bahawa salah satu atom oksigen membentuk ikatan dengan orbital "d" iodin, yang sebenarnya merupakan hibridisasi sp3d2 (iodin boleh mempunyai orbital "d" yang memperluaskan shell valencenya).
Kristal garam ini dapat menjalani peralihan fasa struktur (pengaturan lain daripada monoklinik) sebagai akibat dari keadaan fizikal yang berbeza yang menundukkan mereka.
Kegunaan dan penggunaan kalium iodate
Penggunaan terapeutik
Iodate kalium biasanya digunakan untuk mencegah pengumpulan radioaktiviti dalam tiroid dalam bentuk 131Saya, apabila isotop ini digunakan dalam penentuan pengambilan iodin oleh tiroid sebagai komponen fungsi kelenjar tiroid.
Begitu juga, potassium iodate digunakan sebagai antiseptik topikal (0.5%) dalam jangkitan mukosa.
Gunakan dalam industri
Ia ditambah kepada makanan haiwan ternakan sebagai tambahan iodin. Oleh itu, dalam industri potassium iodate digunakan untuk meningkatkan kualiti tepung.
Penggunaan analitik
Dalam kimia analisis, terima kasih kepada kestabilannya, ia digunakan sebagai standard utama dalam penyeragaman larutan standard natrium thiosulfate (Na2S2O3), untuk menentukan kepekatan yodium dalam sampel.
Ini bermakna jumlah yodium boleh diketahui dengan teknik volumetrik (titrasi). Dalam reaksi ini, potassium iodate dengan cepat mengoksidakan ion iodida I-, dengan persamaan kimia berikut:
IO3- + 5I- + 6H+ => 3I2 + 3H2O
Iodin, saya2, bertajuk dengan penyelesaian Na2S2O3 untuk penyeragamannya.
Digunakan dalam teknologi laser
Kajian telah menunjukkan dan mengesahkan menarik sifat piezoelektrik, pyroelectric, electrooptical, kristal ferroelektrik dan bukan linear optik KIO3. Ini menghasilkan potensi besar dalam bidang elektronik dan teknologi laser untuk bahan yang dibuat dengan sebatian ini.
Risiko kesihatan kalium iodate
Dalam dos yang tinggi boleh menyebabkan kerengsaan pada mukosa lisan, kulit, mata dan saluran pernafasan.
Eksperimen ketoksikan kalium iodate pada haiwan telah dibenarkan untuk memerhatikan bahawa dalam berpuasa anjing pada dos 0,2-0,25 g / kg berat badan, yang disampaikan secara lisan, ia menyebabkan sebatian muntah.
Sekiranya muntah-muntah ini dielakkan, ia akan menyebabkan keadaan menjadi teruk dalam haiwan, kerana ia menyebabkan anoreksia dan sujud sebelum kematian. Autopsi beliau dibenarkan untuk mematuhi lesi nekrotik di hati, buah pinggang dan mukosa usus.
Oleh kerana kuasa pengoksidaannya, ia mewakili risiko kebakaran ketika bersentuhan dengan bahan mudah terbakar.
Rujukan
- Hari, R., & Underwood, A. Kimia Analisis Kuantitatif (edisi kelima). Dewan Prentice PEARSON, p-364.
- Muth, D. (2008). Laser. [Rajah]. Diperolehi daripada: flickr.com
- ChemicalBook. (2017). Kalium iodate. Diperoleh pada 25 Mac, 2018, dari ChemicalBook: chemicalbook.com
- PubChem. (2018). Potassium Iodate. Diperoleh pada 25 Mac, 2018, dari PubChem: pubchem.ncbi.nlm.nih.gov
- Merck. (2018). Kalium iodate. Diambil pada 25 Mac, 2018, dari Merck:
- merckmillipore.com
- Wikipedia. (2017). Kalium iodate. Diperoleh pada 25 Mac, 2018, dari Wikipedia: en.wikipedia.org
- M M Abdel Kader et al. (2013). Mekanisme pengangkutan caj dan peralihan fasa suhu rendah di KIO3. J. Phys .: Conf. Ser 423 012036


