Strontium hydroxide (Sr (OH) ₂) struktur kimia, sifat dan kegunaan
The strontium hidroksida (Sr (OH) ₂) adalah sebatian kimia anorganik yang terdiri daripada ion strontium (Sr) dan dua ion hidroksida (OH). Kompaun ini diperolehi dengan menggabungkan garam strontium dengan pangkalan yang kuat, mengakibatkan sebatian sifat alkali yang formula kimianya adalah Sr (OH)2.
Secara umum, natrium hidroksida (NaOH) atau kalium hidroksida (KOH) digunakan sebagai asas yang kukuh untuk penyediaan strontium hidroksida. Sebaliknya, garam strontium (atau strontium ion) yang bertindak balas dengan asas yang kuat adalah strontium nitrat Sr (NO3)2 dan prosesnya diterangkan oleh reaksi kimia berikut:
2KOH + Sr (NO3)2 → 2KNO3 + Sr (OH)2
Dalam penyelesaian strontium kation (Sr+) disentuh dengan anion hidroksida (OH-) membentuk garam ionik asas strontium. Oleh kerana strontium adalah logam alkali tanah, strontium hidroksida dianggap sebagai sebatian alkali kaustik.
Indeks
- 1 Mendapatkan
- 2 Struktur kimia dan sifat fizikokimia
- 2.1 Strontium Hydroxide Octahydrate
- 2.2 Strontium hidroksida monohidrat
- 2.3 Strontium hydroxide tanpa asid
- 2.4 Kelarutan
- 2.5 Kereaktifan kimia
- 3 Kegunaan
- 3.1 Pengekstrakan molases dan penambahan bit gula
- 3.2 Strontium lemak
- 3.3 Penstabil plastik
- 3.4 Aplikasi lain
- 4 Rujukan
Mendapatkan
Sebagai tambahan kepada proses yang dijelaskan sebelumnya, dapat dikatakan bahawa apabila reaksi telah dilakukan, Sr (OH)2 menjejaskan penyelesaian. Kemudian ia tertakluk kepada proses pencucian dan pengeringan, akhirnya mendapatkan serbuk putih yang sangat halus.
Kaedah alternatif untuk mendapatkan strontium hidroksida adalah dari pemanasan strontium karbonat (SrCO)3) atau strontium sulfat (SrSO)4) dengan stim pada suhu antara 500 ° C dan 600 ° C. Reaksi kimia berlaku seperti yang ditunjukkan di bawah:
SrCO3 + H2O → Sr (OH)2 + CO2
SrS + 2H2O → Sr (OH)2 + H2S
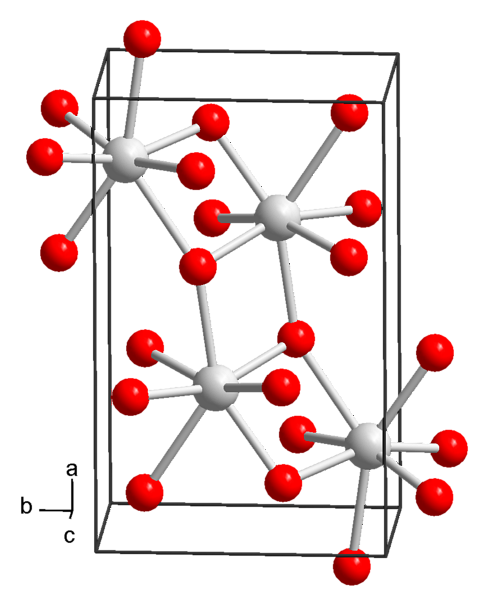
Struktur kimia dan sifat fizikokimia
Pada masa ini 3 bentuk strontium hidroksida diketahui: oktahidrat, monohidrat dan anhidrat.
Strontium Hydroxide Octahydrate
Daripada penyelesaian di bawah keadaan normal suhu dan tekanan (25 ° C dan 1 atm), strontium hidroksida akan merangsang dalam bentuk oktahidrasi, yang formula kimianya ialah Sr (OH)2∙ 8H2O.
Kompaun ini mempunyai jisim molar 265,76 g / mol, ketumpatan 1.90 g / cm dan dicetuskan sebagai kristal tetragonal (dengan kumpulan ruang P4 / NCC) penampilan prismatic berbentuk empat berwarna.
Juga, strontium hidroksida oktahidrat mempunyai keupayaan untuk menyerap kelembapan atmosfera, kerana ia adalah sebatian mudah.
Strontium hydroxide monohydrate
Menurut kajian mikroskopi optik (dilakukan dengan teknik difraksi sinar-X), dengan menaikkan suhu kepada kira-kira 210 ° C - pada tekanan atmosfera yang berterusan - Sr (OH)2∙ 8H2Atau dehidrasi dan diubah menjadi strontium hidroksida monohidrat (Sr (OH)2∙ H2O).
Bentuk sebatian ini mempunyai jisim molar 139.65 g / mol dan suhu leburnya ialah -73.15 ° C (375K). Oleh kerana konfigurasi atomnya, ia memberikan kelarutan yang lebih rendah dalam air daripada yang diterangkan dalam bentuk oktahidrasinya.
Anhydrous strontium hydroxide
Dengan terus meningkatkan suhu sistem kepada kira-kira 480 ° C, dehidrasi berterusan sehingga strontium hidroksida anhidrat diperoleh.
Tidak seperti bentuk terhidratnya, ia mempunyai jisim molar sebanyak 121.63 g / mol dan ketumpatan 3.625 g / cm3. takat didih dicapai pada 710 ° C (1310 ° F atau 983 K) manakala takat lebur 535 ° C (995 ° F atau 808 K).
Kelarutan
The octahydrate strontium hidroksida mempunyai kelarutan dalam air 0.91 gram bagi setiap 100 mililiter (diukur pada 0 ° C), manakala bentuk anhydrous kepada keadaan yang sama suhu mempunyai keterlarutan 0.41 gram bagi setiap 100 mililiter.
Dengan cara yang sama, bahan ini dianggap tidak larut dalam aseton dan sepenuhnya larut dalam asid dan ammonium klorida.
Kereaktifan kimia
Strontium hidroksida adalah tidak mudah menyala, kereaktifan kimia kekal stabil pada suhu sederhana dan tekanan, dan mampu menyerap karbon dioksida daripada udara atmosfera, mengubahnya menjadi strontium karbonat.
Di samping itu, ia adalah sebatian yang sangat menjengkelkan jika ia bersentuhan dengan kulit, saluran pernafasan atau kawasan mukus lain badan.
Kegunaan
Oleh kerana ciri-ciri dan ciri-ciri asasnya, strontium hidroksida digunakan untuk aplikasi yang berlainan dalam industri:
- Pengekstrakan molases dan penapisan gula daripada bit.
- Penstabil plastik.
- Grease dan pelincir.
Pengekstrakan molases dan penambahan bit gula
Pada awal abad XXI di Jerman ia mula menggunakan strontium hidroksida untuk gula penapisan dari bit melalui proses yang dipatenkan oleh Carl Scheibler pada tahun 1882.
Proses ini terdiri daripada campuran strontium hidroksida dan pulpa gula bit, yang mengakibatkan disakarida tidak larut. Penyelesaian ini dipisahkan dengan decanting dan setelah proses penyulingan dilakukan, gula diperolehi sebagai produk akhir.
Walaupun prosedur ini masih digunakan hari ini, terdapat kaedah-kaedah lain dengan lebih banyak permintaan, kerana mereka lebih murah, yang digunakan di sebagian besar kilang gula di dunia. Sebagai contoh, kaedah Barsil, yang menggunakan kaedah barium silicate atau kaedah steffen menggunakan Cal sebagai agen pengekstraksinya.
Strontium greases
Mereka adalah pelincir gris yang mengandungi strontium hidroksida. Ini dapat mematuhi dengan kuat ke permukaan dengan ciri-ciri logam, tahan terhadap air dan menahan perubahan mendadak dalam suhu.
Oleh kerana kestabilan fizikal dan kimia yang baik, lemak ini digunakan sebagai pelincir industri.
Penstabil plastik
Sebahagian besar plastik apabila terdedah kepada faktor cuaca seperti matahari, hujan dan oksigen atmosfera, mengubah sifat dan kemerosotan sifatnya.
Oleh rintangan air yang besar, strontium hidroksida ditambah kepada polimer ini -Semasa fasa Fusion-bertindak sebagai penstabil dalam pembuatan produk plastik untuk memanjangkan jangka hayat mereka.
Permohonan lain
- Dalam industri cat, ia digunakan sebagai tambahan penting untuk mempercepatkan proses pengeringan dalam cat komersial dan industri.
- Garam strontium atau ion strontium diperolehi daripada strontium hidroksida dan digunakan sebagai bahan mentah untuk pengeluaran artikel piroteknik.
Rujukan
- Wikipedia. (n.d.). Strontium hydroxide. Diambil dari en.wikipedia.org
- PubChem. (s.f.). Strontium Hydroxide. Diambil dari pubchem.ncbi.nlm.nih.gov
- Lambert, I. dan Pandai, H. L. (2013). Alkali Bumi Hidroksida dalam Penyelesaian Air dan Berair. Diperoleh dari books.google.com
- Krebs, R. E. (2006). Sejarah dan Penggunaan Elemen Kimia Bumi Kita: Panduan Rujukan. Diperoleh dari books.google.com
- Honeywell (s.f.). Strontium Hydroxide Octahydrate. Pulih dari honeywell.com


