Struktur, sifat, nomenklatur dan kegunaan perak oksida (Ag2O)
The perak oksida adalah sebatian organik yang formula kimianya adalah Ag2O. Daya yang menyatukan atomnya adalah sifat ionik sepenuhnya; Oleh itu, ia terdiri daripada pepejal ionik di mana terdapat dua kation Ag+ berinteraksi dengan elektrostatik dengan anion O2-.
Anion oksida, O2-, ia hasil dari interaksi atom perak permukaan dengan oksigen alam sekitar; dengan cara yang sangat serupa untuk besi dan banyak logam lain. Sekeping perak atau perhiasan dan bukannya kemerahan dan runtuh ke karat, bertukar hitam, ciri perak oksida.

Sebagai contoh, dalam imej di atas anda dapat melihat cawan perak berkarat. Perhatikan permukaannya yang hitam, walaupun masih mengekalkan beberapa kilauan hiasan; itulah sebabnya walaupun objek perak berkarat boleh dianggap cukup menarik untuk digunakan hiasan.
Sifat-sifat oksida perak sedemikian rupa sehingga tidak merosakkan, pada pandangan pertama, permukaan logam asal. Ia terbentuk pada suhu bilik dengan sentuhan mudah dengan oksigen di udara; dan lebih menarik lagi, ia boleh terurai pada suhu tinggi (di atas 200 ° C).
Ini bererti bahawa jika kaca imej itu dipegang, dan api panas yang kuat digunakan, ia akan memulihkan kilauan keperakannya. Oleh itu, pembentukannya adalah proses termodinamik yang boleh dibalikkan.
Oksida perak juga mempunyai sifat-sifat lain dan, di luar formula Ag sederhana2Atau, ia merangkumi organisasi struktur yang kompleks dan pelbagai jenis pepejal yang kaya. Walau bagaimanapun, Ag2Atau mungkin, di sebelah Ag2O3, yang paling mewakili oksida perak.
Indeks
- 1 Struktur perak oksida
- 1.1 Perubahan dengan bilangan valencia
- 2 Sifat fizikal dan kimia
- 2.1 Berat molekul
- 2.2 Penampilan
- 2.3 Ketumpatan
- 2.4 Tahap lebur
- 2.5 Kps
- 2.6 Keterlarutan
- 2.7 Watak kovalen
- 2.8 Penguraian
- 3 Nomenklatur
- 3.1 Valencias I dan III
- 3.2 Tatanama sistematik untuk oksida perak kompleks
- 4 Kegunaan
- 5 Rujukan
Struktur perak oksida
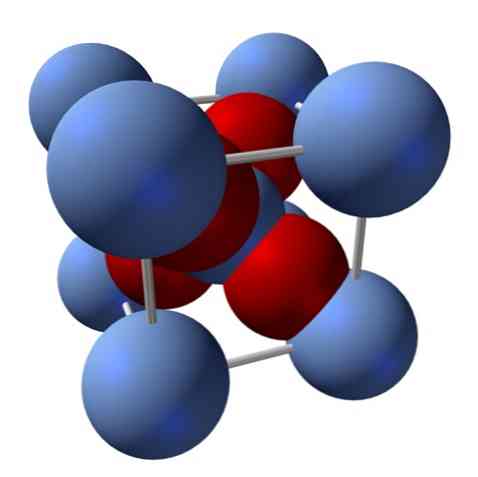
Bagaimana strukturnya? Seperti yang dinyatakan pada permulaan: ia adalah pepejal ionik. Atas sebab ini, tidak ada ikatan kovalen Ag - O atau Ag = O dalam strukturnya; kerana, jika ada, sifat oksida ini akan berubah secara drastik. Ini kemudiannya Ag ion+ dan O2- dalam nisbah 2: 1 dan mengalami tarikan elektrostatik.
Struktur oksida perak ditentukan dengan cara di mana daya ionik dibuang di dalam ruang Ag ion+ dan O2-.
Di bahagian atas imej, sebagai contoh, anda mempunyai sel unit untuk sistem kristal padu: kation Ag+ adalah sfera perak biru, dan O2- sfera kemerahan.
Sekiranya anda mengira jumlah sfera, anda akan mendapati bahawa terdapat sekilas pandang, sembilan keperakan biru dan empat warna merah. Bagaimanapun, hanya serpihan sfera yang terkandung dalam kiub itu diambil kira; daripada mengira ini, sebagai pecahan dari total sfera, nisbah 2: 1 untuk Ag mesti dipenuhi2O.
Mengulangi unit struktur tetrahedron AgO4 dikelilingi oleh empat lagi Ag+, semua pepejal hitam dibina (menanggalkan jurang atau penyelewengan yang boleh dibuat oleh kristal ini).
Perubahan dengan jumlah valencia
Memfokus sekarang bukan pada tetrahedron AgO4 tetapi dalam garisan AgOAg (perhatikan simpul atas kiub atas), maka akan menjadi pepejal oksida perak terdiri dari perspektif lain, lapisan ion berganda yang linear (walaupun cenderung). Semua ini sebagai akibat daripada geometri "molekul" di sekitar Ag+.
Di atas telah disokong oleh beberapa kajian struktur ioniknya.
Perak bekerja terutamanya dengan valence +1, kerana apabila kehilangan elektron konfigurasi elektronik yang terhasil ialah [Kr] 4d10, yang sangat stabil. Valensi lain, seperti Ag2+ dan Ag3+ mereka kurang stabil kerana mereka kehilangan elektron daripada orbital hampir penuh.
The Ag3+, Walau bagaimanapun, ia agak kurang tidak stabil berbanding dengan Ag2+. Malah, ia boleh wujud bersama syarikat Ag+ Kimia memperkayakan struktur.
Konfigurasi elektroniknya ialah [Kr] 4d8, dengan elektron yang tidak berpasangan sedemikian rupa sehingga memberikannya beberapa kestabilan.
Tidak seperti geometri linear di sekitar Ag Ag+, telah dijumpai bahawa ion Ag3+ Ia persegi rata. Oleh itu, oksida perak dengan ion Ag3+ akan terdiri daripada lapisan yang terdiri daripada dataran AgO4 (bukan tetrahedra) disambung secara elektrostat oleh garisan AgOAg; Begitulah kes Ag4O4 Ag2O ∙ Ag2O3 dengan struktur monoklinik.
Sifat fizikal dan kimia

Sekiranya anda menggaru permukaan cawan perak dari imej utama, anda akan mendapat padu, yang bukan hanya hitam, tetapi juga mempunyai nada coklat atau coklat (imej atas). Beberapa sifat fizikal dan kimia yang dilaporkan oleh momen adalah seperti berikut:
Berat molekul
231,735 g / mol
Rupa
Bentuk coklat hitam pepejal dalam bentuk serbuk (ambil perhatian bahawa walaupun pepejal ionik, ia tidak mempunyai rupa kristal). Ia tidak berbau dan bercampur dengan air memberikannya rasa logam
Ketumpatan
7.14 g / mL.
Titik lebur
277-300 ° C. Sudah tentu, ia cair ke dalam perak yang padat; iaitu, ia mungkin rosak sebelum membentuk oksida cecair.
Kps
1.52 ∙ 10-8 dalam air pada 20 ° C. Oleh itu, ia adalah sebatian yang agak larut dalam air.
Kelarutan
Jika anda melihat dengan teliti pada imej strukturnya, anda akan mendapati bahawa bidang Ag2+ dan O2- Mereka tidak bersetuju dengan saiznya. Akibatnya, hanya molekul kecil boleh menembus bahagian dalam kisi kristal, menjadikannya tidak larut dalam hampir semua pelarut; kecuali bagi orang-orang di mana ia bertindak balas, seperti asas dan asid.
Watak kovalen
Walaupun ia telah dikatakan berulang kali bahawa oksida perak adalah sebatian ionik, sifat-sifat tertentu, seperti titik leburnya yang rendah, bercanggah dengan pernyataan ini.
Sudah tentu, pertimbangan watak kovalen tidak memecahkan apa yang dijelaskan untuk strukturnya, ia akan mencukupi untuk menambahnya kepada struktur Ag2Atau model sfera dan bar untuk menunjukkan ikatan kovalen.
Juga, tetrahedra dan pesawat persegi AgO4, serta garisan AgOAg, mereka akan dikaitkan dengan ikatan kovalen (atau ion kovalen).
Dengan ini, Ag2Atau ia sebenarnya akan menjadi polimer. Walau bagaimanapun, adalah disyorkan untuk menganggapnya sebagai pepejal ionik dengan watak kovalen (yang sifat pautannya masih menjadi cabaran pada masa kini).
Penguraian
Pada mulanya disebutkan bahawa pembentukannya termodinamik boleh diubah, jadi ia menyerap haba untuk kembali ke keadaan logamnya. Semua ini boleh dinyatakan oleh dua persamaan kimia untuk tindak balas tersebut:
4Ag (s) + O2(g) => 2Ag2O (s) + Q
2Ag2O (s) + Q => 4Ag (s) + O2(g)
Di mana Q mewakili haba dalam persamaan. Ini menjelaskan mengapa api membakar permukaan cawan perak berkarat mengembalikan keperakan keperakannya.
Oleh itu, sukar untuk mengandaikan bahawa terdapat Ag2O (1) kerana ia akan terurai dengan serta-merta dengan haba; melainkan tekanan terlalu tinggi untuk mendapatkan cecair hitam coklat tersebut.
Tatanama
Apabila kemungkinan Ag ion diperkenalkan2+ dan Ag3+ selain Ag yang biasa dan dominan+, istilah 'oksida perak' mula kelihatan tidak mencukupi untuk merujuk kepada Ag2O.
Ini adalah kerana Ag+ lebih banyak daripada yang lain, jadi Ag diambil2Atau sebagai satu-satunya oksida; yang tidak betul sama sekali.
Jika anda menganggap Ag2+ seperti tidak praktikal yang diberikan ketidakstabilannya, maka hanya ion dengan valensi +1 dan +3 akan hadir; iaitu, Ag (I) dan Ag (III).
Valencias I dan III
Sebagai Ag (I) yang paling sedikit valensi, ia dinamakan dengan menambah sufiks -oso kepada namanya argentum. Oleh itu, Ag2Atau ia adalah: argentoso oxide atau, menurut tatanama yang sistematik, diplata monoksida.
Jika Ag (III) diabaikan sepenuhnya, tatanama tradisionalnya mestilah: oksida perak bukannya oksida argentine.
Sebaliknya, Ag (III) menjadi valensi yang lebih besar ditambah akhiran -ico dengan namanya. Oleh itu, Ag2O3 adalah: oksida perak (2 Ag ion)3+ dengan tiga O2-). Juga namanya mengikut tatanama yang sistematik ialah: diplata trioksida.
Sekiranya struktur Ag diperhatikan2O3, ia boleh dianggap bahawa ia adalah hasil pengoksidaan oleh ozon, ATAU3, bukan oksigen. Oleh itu, sifat kovalennya mesti lebih besar kerana ia adalah sebatian kovalen dengan bon Ag-O-O-O-Ag atau Ag-O.3-Ag.
Tatanama sistematik untuk oksida perak kompleks
The AgO, juga ditulis sebagai Ag4O4 Ag2O ∙ Ag2O3, ia adalah oksida perak (I, III), kerana ia mempunyai kedua-dua valensi +1 dan +3. Namanya mengikut tatanama yang sistematik ialah: tetraplate tetraoksida.
Nomenklatur ini sangat membantu apabila datang kepada oksida perak yang lebih kompleks lagi stoikiometrik. Sebagai contoh, katakan dua pepejal 2Ag2O ∙ Ag2O3 dan Ag2O ∙ 3Ag2O3.
Menulis yang pertama dengan cara yang lebih sesuai ialah: Ag6O5 (mengira dan menambah atom Ag dan O). Namanya akan menjadi hexaplate pentoxide. Perhatikan bahawa oksida ini mempunyai komposisi perak yang kurang kaya daripada Ag2O (6: 5 < 2:1).
Semasa menulis pepejal kedua sebaliknya, ia akan menjadi: Ag8O10. Namanya akan menjadi octaplate decaoxide (dengan nisbah 8:10 atau 4: 5). Ini perak oksida hipotetikal akan "sangat teroksida".
Kegunaan
Kajian untuk mencari kegunaan baru dan canggih untuk perak oksida masih dijalankan hari ini. Beberapa kegunaannya disenaraikan di bawah:
-Ia dibubarkan dalam ammonia, ammonium nitrat dan air untuk membentuk reaksi Tollens. Reagen ini adalah alat yang berguna dalam analisis kualitatif dalam makmal kimia organik. Ia membolehkan untuk menentukan kehadiran aldehid dalam sampel, tindak balas positif ialah pembentukan "cermin perak" dalam tiub ujian.
-Bersama zink logam ia membentuk bateri utama zink-oksida perak. Ini mungkin salah satu kegunaan yang paling biasa dan homelike.
-Ia berfungsi sebagai pembersih gas, menyerap contohnya CO2. Apabila dipanaskan, ia melepaskan gas yang terperangkap dan boleh digunakan semula beberapa kali.
-Disebabkan sifat antimikrobial perak, oksidanya berguna dalam kajian bioanalisis dan pembersihan tanah.
-Ia adalah agen pengoksidaan ringan yang mampu mengoksidasi aldehida kepada asid karboksilik. Ia juga digunakan dalam reaksi Hofmann (amina tersier) dan mengambil bahagian dalam reaksi organik yang lain, sama ada sebagai reagen atau pemangkin.
Rujukan
- Bergstresser M. (2018). Perak Oxide: Formula, Penguraian & Pembentukan. Kajian. Diperolehi daripada: study.com
- Penulis dan pengarang volum III / 17E-17F-41C. (s.f.). Perak oksida (Ag (x) O (y)) struktur kristal, parameter kekisi. (Data Berangka dan Hubungan Fungsian dalam Sains dan Teknologi), jilid 41C. Springer, Berlin, Heidelberg.
- Mahendra Kumar Trivedi, Rama Mohan Tallapragada, Alice Branton, Dahryn Trivedi, Gopal Nayak, Omprakash Latiyal, Snehasis Jana. (2015). Kesan Potensi Energy Rawatan biofield atas Sifat Fizikal dan Thermal perak oksida serbuk. Jurnal Antarabangsa Sains dan Kejuruteraan Bioperubatan. Vol. 3, No. 5, ms. 62-68. doi: 10,11648 / j.ijbse.20150305.11
- Sullivan R. (2012). Penguraian oksida perak. Universiti Oregon Diperolehi daripada: chemdemos.uoregon.edu
- Flint, Deyanda. (24 April 2014). Penggunaan Bateri Perak Oksida. Saintifik. Diperolehi daripada: sciencing.com
- Salman Montasir E. (2016). Kajian Beberapa sifat optik perak oksida (Ag2o) menggunakan spektrofotometer UVVisible. [PDF] Diperolehi daripada: iosrjournals.org
- Bard Allen J. (1985). Potensi Standard dalam Penyelesaian Berair. Marcel Dekker. Diperolehi daripada: books.google.com.ve


