Asas gram, bahan, teknik dan kegunaan Gram
The Gram noda adalah teknik pewarnaan paling mudah dan paling berguna dalam mikrobiologi diagnostik. Teknik ini dicipta oleh doktor Denmark, Hans Christian Gram pada tahun 1884, yang berjaya mengklasifikasikan bakteria dalam Gram positif dan Gram negatif, menurut komposisi dinding sel.
Teknik ini menjalani pengubahsuaian tertentu oleh Hucker pada tahun 1921 untuk menstabilkan reagen-reagen dan meningkatkan kualiti noda, supaya gram Gram juga dikenali sebagai Gram-Hucker.
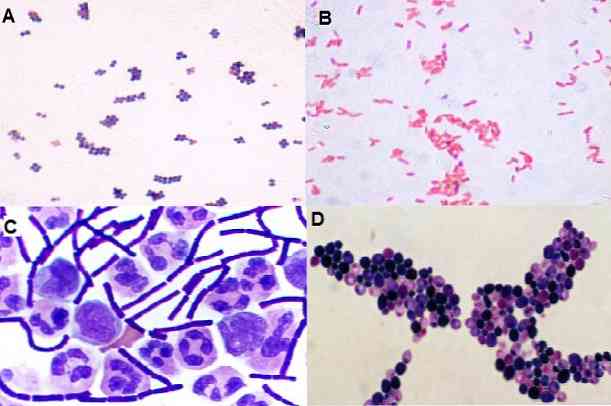
Dengan teknik ini juga mungkin untuk melihat bentuk yang terdapat dalam mikroorganisma, sama ada mereka cocci, bacilli, coccobacilli, pleomorphic, filamentous, antara lain. Serta pengedarannya di angkasa: dalam kelompok, dalam rantai, terpencil, berpasangan, dalam tetrads, dan lain-lain.
Apabila jangkitan bakteria disyaki, kebanyakan sampel yang diterima harus tersebar di atas slaid dan diwarnai dengan Gram untuk pemeriksaan di bawah mikroskop..
Laporan Gram akan membimbing doktor tentang apa jenis mikroorganisma boleh menjadi punca jangkitan, sebelum mendapatkan hasil akhir tanaman.
Dalam sesetengah kes, kehidupan pesakit sangat dikompromi, jadi doktor segera memerlukan laporan Gram untuk meletakkan rawatan empirik, sambil menunggu identifikasi mikroorganisma.
Sebagai contoh, jika Gram mendedahkan bahawa terdapat cocci Gram positif dalam cecair cerebrospinal, doktor akan mengorientasikan terapi awal dengan antibiotik yang menghilangkan bakteria jenis ini, menurut protokol yang ditetapkan untuknya..
Apabila hasil akhir tiba dengan nama mikroorganisma yang terpencil dan antibiogram masing-masing, doktor akan menilai sama ada untuk mengubah terapi tersebut. Keputusan ini akan dibuat menurut kajian kerentanan mikroorganisma kepada antibiotik yang ia terima dan evolusi pesakit.
Indeks
- 1 Yayasan
- 2 Bahan
- 3 Penyediaan pewarna dan reagen
- 3.1 penyelesaian kristal violet
- 3.2 Iodo-Lugol
- 3.3 Pelunturan
- 3.4 Sebaliknya
- 4 Penyimpanan reagen
- 5 Penyediaan penyebaran sampel berwarna
- 5.1 -Gram sampel langsung
- 5.2 -Gram tanaman
- 6 Teknik
- 7 Utiliti
- 8 Kesilapan biasa
- 9 Rujukan
Yayasan
Ini adalah teknik yang membentangkan 4 langkah asas: pewarnaan, penetapan dengan mordan, perubahan warna dan kontrasepsi. Oleh itu, teknik ini selain mewarna bakteria, juga membezakannya.
Violet kristal adalah pewarna pertama yang digunakan. Ia mempunyai pertalian untuk peptidoglycan dan noda ungu semua bakteria kemudian Lugol, yang bertindak sebagai pedas, yang diletakkan, akan mendorong pembentukan kompleks larut kristal ungu-iodin - protein ribonuclear dalam sel.
Bakteria gram-positif, mempunyai dinding peptidoglycan tebal, membentuk lebih kompleks (kristal ungu-iodin), oleh itu mereka mengekalkan pewarna.
Ia juga mempengaruhi bahawa bakteria Gram-positif dinding mengandungi lebih banyak asid tak tepu, yang menunjukkan pertalian yang tinggi untuk agen pengoksida (Lugol).
Sementara itu, bakteria Gram-negatif mempunyai lapisan peptidoglycan yang nipis, yang menjadikan bakteria kurang kompleks daripada bakteria Gram-positif.
Kemudian datang langkah perubahan warna, di mana bakteria Gram positif dan Gram negatif bertindak berbeza.
Bakteria gram negatif mengandungi membran luar yang kaya dengan lipopolisakarida yang merupakan sebahagian daripada dinding selnya. Lemak dimusnahkan dengan bersentuhan dengan aseton alkohol, jadi membran luar tidak stabil, kristal ungu dilepaskan.
Ini adalah bagaimana ia dihitung dengan safranin atau fuchsin asas, mengambil warna merah.
Dalam kes bakteria Gram-positif, mereka menolak perubahan warna kerana peluntur bertindak untuk menutup liang-liang, yang menghalang kompleks kristal ungu / yodium dari melarikan diri.
Oleh itu, pewarna dengan kristal ungu stabil, dan tidak ada ruang untuk safranin atau fuchsin. Oleh itu, bakteria ini mencemarkan warna biru atau ungu yang sengit.
Bahan
Kumpulan pewarna Gram terdiri daripada:
- Kristal violet
- Lugol
- Alkohol aseton
- Safranin atau fuchsin asas
Penyediaan pewarna dan reagen
Penyelesaian ungu Kristal
Penyelesaian A:
Kristal violet -2 gr
Etil alkohol 95% -20cc
Penyelesaian B:
Ammonium oxalate -0.8 gr
Air suling-80 cc
Untuk penyediaan akhir kristal ungu, larutan 1:10 harus dicairkan dengan air suling dan dicampurkan dengan 4 bahagian larutan B. Campuran disimpan selama 24 jam sebelum digunakan. Ia ditapis dalam botol untuk pewarnaan ambar menggunakan penapis kertas.
Jumlah yang akan digunakan setiap hari dipindahkan ke botol amber dengan penitis.
Iodo-Lugol
Timbang dan ukur jumlah yang dinyatakan setiap kompaun, seperti berikut:
Kristal Iodo - 1 gr
Potassium Iodide - 2 gr
Air suling -300 cc
Iodida kalium larut sedikit demi sedikit di dalam air dan kemudian iodin ditambah. Penyelesaiannya dicukur dengan botol berwarna ambar.
Jumlah yang akan digunakan setiap hari dipindahkan ke botol ambar yang lebih kecil dengan penitis.
Pemutihan
95% etil alkohol -50 ml
Acetone - 50 ml
Ia disediakan dalam bahagian yang sama. Tutup dengan baik, ia cenderung untuk menguap.
Letakkan dalam botol dengan penitis.
Penyediaan ini memberikan perubahan warna dalam masa sederhana 5-10 saat dan adalah yang paling disyorkan.
Pemula lebih suka menggunakan hanya 95% etil alkohol, di mana perubahan warna lebih perlahan daripada 10 hingga 30 saat.
Walaupun yang paling berpengalaman boleh menggunakan aseton tulen, di mana perubahan warna berlaku dengan cepat dari 1 hingga 5 saat.
Sebaliknya
Penyelesaian stok Safranin
Safranina -2.5 gr
Etil alkohol 95% -100 cc
Selepas menimbang jumlah yang ditunjukkan safranin larut dalam 100 cc etil alkohol hingga 95%.
Penyelesaian safranin bekerja disediakan dari penyelesaian stok.
Untuk melakukan ini, ukur 10 cc penyelesaian stok, tambah 90 cc air suling untuk menyelesaikan 100 ml.
Adalah disyorkan untuk memindahkan jumlah yang akan digunakan setiap hari untuk botol ambar dengan penitis.
Mikroorganisma yang noda lemah Gram-negatif dengan Gram-Hucker noda, seperti anaerob tertentu, Legionella sp, Campylobacter sp dan Brucella sp, mereka boleh menjadi lebih baik lagi jika pengubahsuaian yang dibuat oleh Kopeloff kepada Gram-Hucker pewarnaan, yang dipanggil Gram-Kopeloff noda, digunakan.
Teknik ini mengubah pewarna safranin dengan fuchsin asas. Dengan pengubahsuaian ini adalah mungkin untuk mengukur mikroorganisma yang dinyatakan di atas.
Penyimpanan reagen
Pewarna yang disiapkan perlu disimpan pada suhu bilik.
Penyediaan sampel tersebar ke warna
Sampel mesti mengandungi sekurang-kurangnya 105 Mikroorganisma sebelum pemerhatian mikroorganisma dalam smear mungkin. Spread boleh dibuat dari sampel langsung atau budaya dalam media pepejal atau cecair.
Sebaran harus seragam, teragih dan tidak terlalu tebal, untuk visualisasi struktur yang lebih baik.
-Gram sampel langsung
Gram urin tanpa centrifuge
Urin bercampur dan 10 μl diletakkan pada slaid. Observasi sekurang-kurangnya satu bakteria / medan Penyerapan menunjukkan bahawa terdapat jangkitan.
Ini bermakna bahawa budaya akan mempunyai lebih kurang 100,000 CFU / ml (105 CFU / mL) dalam 85% kes.
Kaedah ini tidak berguna untuk kiraan koloni di bawah 100,000 CFU.
LCR Gram
CSF perlu disentri, supernatan dikeluarkan dan pelet tersebar di atas slaid. Cecair ini steril dalam keadaan normal; pemerhatian bakteria menunjukkan jangkitan.
Gram sampel pernafasan
Gram sputum, bronkial atau bronchoalveolar lavage, walaupun mungkin terdapat pelbagai mikroorganisma, akan sentiasa membimbing diagnosis, selain berguna jenis sel yang diperhatikan.
Dalam kes dahagakan, pil smear harus disediakan dengan bahagian yang paling purulen dari sampel.
Stool Gram
Ia tidak disyorkan untuk melaksanakan Gram untuk jenis sampel ini, kerana ia tidak mempunyai nilai diagnostik.
-Tanaman Gram
Mereka boleh dilakukan dalam dua cara, satu dari tanaman cair dan satu lagi dari tanaman pepejal.
Tanaman cecair
Dari budaya cecair ia sangat mudah; di bawah beberapa Roasted sup kotor ringan mereka diambil dan diletakkan di atas slaid kering bersih, memberi gerakan membulat dari pusat ke arah pinggir, untuk mengedarkan bahan sama rata.
Ia dibenarkan untuk kering secara spontan di udara. Sebaik sahaja kering, bahan itu dipasang pada lembaran dengan haba. Untuk ini, dengan bantuan pengapit, lembaran 3 diluluskan 4 kali melalui api pembakar Bunsen, berhati-hati untuk tidak membakar bahan.
Lembaran ini dibenarkan untuk menyejukkan dan diletakkan pada jambatan pewarna.
Tanaman pepejal
Untuk melaksanakan lanjutan untuk noda Gram dari budaya pepejal, meneruskan seperti berikut:
Sebelum memilih tanah jajahan yang diambil, slaid perlu disediakan, meletakkan dua titik kira-kira larutan salin fisiologi steril.
Sekiranya plat budaya asli mengandungi beberapa jenis koloni, satu koloni terpencil masing-masing akan dipilih untuk melaksanakan Gram. Setiap koloni akan diambil dengan gelung platinum untuk membubarkannya dalam larutan garam sebelum diletakkan pada slaid.
Pergerakan pekeliling diberikan dari pusat ke pinggir, untuk mengedarkan koloni secara homogen pada slaid..
Ia dibenarkan untuk kering secara spontan di udara. Setelah mengeringkan lembaran dipasang dengan panas, seperti yang dijelaskan di atas (menyala dengan slaid dengan lebih ringan), berhati-hati untuk tidak membakar bahan.
Prosedur ini mesti dilakukan dengan setiap jenis koloni yang berlainan. Di atas sekeping kertas, pesanan diperhatikan harus diperhatikan, sebagai contoh:
Koloni 1: Jajahan beta-hemolytic kuning: Gram-positif cocci diperhatikan dalam kluster
Koloni 2: Koloni krim, tanpa hemolisis: Gram negatif coccobacilli diperhatikan.
Setiap helaian mesti dilabelkan untuk mengetahui apa yang kita saksikan.
Teknik
Teknik pewarnaan Gram sangat mudah dilakukan dan agak murah dan tidak boleh dilepaskan dalam makmal mikrobiologi.
Perkara yang sama seperti berikut:
- Betulkan smear dengan haba dan letakkan di jambatan berwarna.
- Lembaran ditutup sepenuhnya dengan kaca violet selama 1 minit.
- Basuh dengan air. Jangan keringkan
- Tutup plat dengan larutan Lugol, biarkan selama 1 minit. Basuh dengan air. Jangan keringkan.
- Campurkan selama 5-10 saat dengan pergolakan lembut dalam alkohol aseton. Atau letakkan helaian dalam kedudukan tegak dan titisan titisan ejen decolorizing di permukaan sehingga gelas violet yang tersisa diseret. Jangan melebihi.
- Basuh dengan air. Jangan keringkan.
- Gantikan lembaran pada jambatan berwarna dan tutup selama 30 saat dengan safranin (Gram-Hucker) atau 1 min dengan fuchsin asas (Gram-Kopeloff).
- Basuh dengan air
- Benarkan kering secara spontan di udara menegak.
Setelah kering, letakkan 1 drop minyak rendam untuk memerhatikannya di bawah objektif 100X dalam mikroskop optik.
Utiliti
Teknik ini membolehkan membezakan perbezaan morphotype yang paling bakteria.
Ragi juga dibezakan oleh warna ini. Mereka mengambil ungu kristal, iaitu, mereka noda Gram positif.
Sebaliknya, bakteria pembentukan spora positif boleh dibezakan, di mana ruang yang jelas diperhatikan di dalam bacillus, di mana endospora terbentuk, walaupun spora tidak noda dengan baik. Untuk menggunakan spora, teknik lain seperti Shaeffer-Fulton digunakan.
Perlu diperhatikan bahawa kotoran ini tidak berfungsi untuk mewarna semua jenis bakteria, iaitu, terdapat kes-kes di mana pewarnaan tidak berfungsi.
Dalam kes ini, bakteria yang kekurangan dinding sel boleh disebutkan. Sebagai contoh: genus Mycoplasma, spheroplasts, Ureaplasma, L-bentuk dan protoplas.
Ia juga menyerap bakteria yang teruk dengan dinding yang kaya dengan asid miokolic, seperti Mycobacteria dan bakteria intrasel seperti Chlamydias dan Rickettsias.
Ia juga tidak cekap untuk merosakkan bakteria spirochetal.
Terdapat bakteria genus yang sama yang boleh diperhatikan dalam sampel yang sama seperti Gram positif dan sebagai Gram negatif. Apabila ini berlaku, ia disebut pembolehubah Gram noda, yang mungkin disebabkan oleh perubahan dalam nutrien, suhu, pH atau kepekatan elektrolit..
Kesilapan biasa
Bleach berlebihan
Melebih-lebihkan dalam langkah perubahan warna boleh menyebabkan pemerhatian mikroorganisma gram negatif.
Jangan tunggu masa pengeringan yang cukup untuk menambah minyak rendaman:
Kesalahan ini menyebabkan pembentukan micelles lemak yang menjadikannya sukar untuk melihat struktur yang ada sekarang. Ini berlaku apabila minyak bergabung dengan molekul air yang ada di dalam smear.
Membalikkan perintah reagen:
Kesalahan seperti ini akan menyebabkan bakteria Gram-negatif memaparkan ungu, iaitu Gram-positive palsu.
Gunakan tanaman lama (pepejal atau cecair):
Ia boleh menyebabkan bakteria Gram positif untuk mengotorkan Gram negatif (negatif Gram negatif). Ini berlaku kerana dalam budaya lama ada kemungkinan ada bakteria yang mati atau memburuk dan di bawah kondisi ini bakteria tidak mempertahankan kristal ungu.
Gunakan penyelesaian Lugol yang sangat lama:
Lama kelamaan lugol kehilangan sifatnya dan warnanya pudar. Sekiranya reagen yang sudah degenerasi digunakan, ia tidak akan memperbaiki kristal ungu dengan baik, oleh itu terdapat kemungkinan untuk mendapatkan visualisasi mikroorganisma palsu Gram negatif.
Latar belakang Bluish
Latar belakang yang berubah warna akan menjadi merah. Latar belakang biru menunjukkan bahawa perubahan warna tidak mencukupi.
Rujukan
- Ryan KJ, Ray C. 2010. Sherris. Mikrobiologi Perubatan, edisi ke-6 McGraw-Hill, New York, U.S.A
- Koneman E, Allen S, Janda W, Schreckenberger P, Winn W. (2004). Diagnosis mikrobiologi. (Edisi ke-5). Argentina, Editorial Panamericana S.A..
- Forbes B, Sahm D, Weissfeld A. 2009. Diagnosis mikrobiologi Bailey & Scott. 12 ed. Argentina Panamericana S.A Editorial
- Casas-Rincón G. 1994. Mycology Umum. 2nd Ed. Universidad Central de Venezuela, edisi Perpustakaan. Venezuela, Caracas.
- "Gram noda" Wikipedia, ensiklopedia percuma. 4 Okt 2018, 23:40 UTC. 9 Dis 2018, 17:11. Diambil dari es.wikipedia.org.
- González M, González N. 2011. Manual Mikrobiologi Perubatan. Edisi ke-2, Venezuela: Direktorat media dan penerbitan University of Carabobo.
- Lopez-Jácome L, Hernandez-Durán M, C Colin-Castro, Pena-Ortega S, G Ceron-González, pewarna F. Franco-Cendejas asas dalam makmal mikrobiologi. Penyelidikan Hilang Upaya. 2014; 3 (1): 10-18.


