Formula Osmolarity, Cara Menghitung Ia dan Perbezaan dengan Osmolality
The osmolarity adalah parameter yang mengukur kepekatan sebatian kimia dalam satu liter larutan, selagi ia menyumbang kepada sifat colligative yang dikenali sebagai tekanan osmotik penyelesaian tersebut.
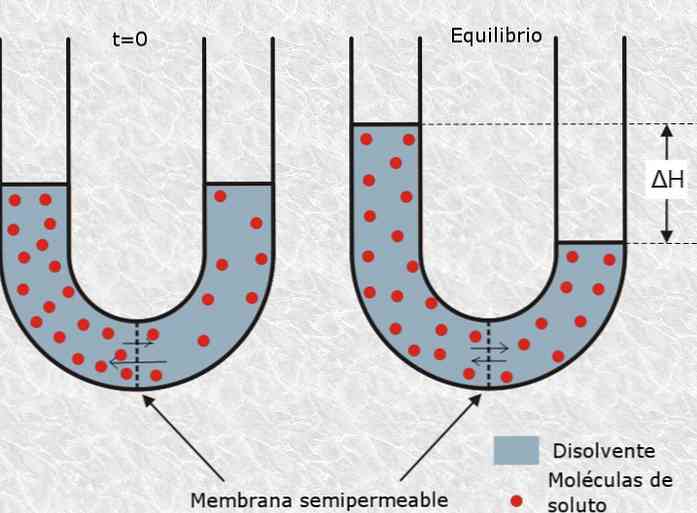
Di sini, tekanan osmosis larutan yang merujuk kepada jumlah tekanan yang diperlukan untuk menghentikan proses osmosis, yang ditakrifkan sebagai laluan terpilih zarah pelarut melalui membran separa telap atau berliang dari penyelesaian daripada kepekatan yang rendah ke yang lebih pekat.
Juga, unit yang digunakan untuk menyatakan jumlah zarah terlarut ialah osmol (simbolnya adalah Osm), yang bukan sebahagian daripada Sistem Sistem Antarabangsa (SI) yang digunakan di hampir seluruh dunia. Oleh itu, kepekatan larut dalam larutan ditakrifkan dalam unit Osmoles seliter (Osm / l).
Indeks
- 1 Formula
- 1.1 Definisi pembolehubah dalam formula osmolarity
- 2 Bagaimana untuk mengiranya?
- 3 Perbezaan antara osmolariti dan osmolality
- 4 Rujukan
Formula
Seperti yang dinyatakan sebelum ini, osmolariti (juga dikenali sebagai kepekatan osmotik) dinyatakan dalam unit yang didefinisikan sebagai Osm / l. Hal ini disebabkan oleh hubungannya dengan penentuan tekanan osmotik dan pengukuran penyebaran pelarut oleh osmosis.
Dalam amalan, kepekatan osmotik boleh ditentukan sebagai kuantiti fizikal dengan penggunaan osmometer.
osmometer adalah alat yang digunakan dalam pengukuran tekanan osmosis penyelesaian, dan penentuan sifat colligative lain (seperti tekanan wap, peningkatan takat didih atau menurunkan takat beku) untuk mendapatkan nilai daripada osmolariti penyelesaian.
Dengan cara ini, untuk mengira parameter ukuran ini, formula berikut digunakan, yang mengambil kira semua faktor yang boleh mempengaruhi harta ini..
Osmolarity = ΣφiniCi
Dalam persamaan ini, osmolariti ditubuhkan sebagai jumlah yang dihasilkan daripada mendarab semua nilai yang diperoleh daripada tiga parameter yang berbeza, yang akan ditakrifkan di bawah.
Definisi pembolehubah dalam formula osmolarity
Pertama pekali osmosis, diwakili oleh huruf Yunani φ (phi), yang menjelaskan berapa banyak tingkah laku penyelesaian yang ideal atau, dalam erti kata lain, tahap bukan idealistis yang nyata bahan larut dalam penyelesaian adalah jauh.
Dengan cara yang paling sederhana, φ merujuk kepada tahap pemisahan larut, yang boleh mempunyai nilai antara sifar dan satu, di mana nilai maksima unit mewakili pemisahan 100%; iaitu, mutlak.
Dalam beberapa kes-sama seperti sukrosa- nilai ini melebihi perpaduan; manakala dalam hal lain, seperti garam, pengaruh interaksi elektrostatik atau taktik menyebabkan pekali osmotik dengan nilai yang kurang daripada perpaduan, walaupun pembubaran mutlak berlaku.
Sebaliknya, nilai n menunjukkan jumlah zarah di mana molekul boleh dipisahkan. Dalam kes spesies ionik, natrium klorida (NaCl), yang nilai n adalah sama dengan dua, diberikan sebagai contoh; sedangkan dalam molekul glukosa yang tidak terion, nilai n adalah sama dengan satu.
Akhirnya, nilai c mewakili kepekatan larut, dinyatakan dalam unit molar; dan subskrip saya merujuk kepada identiti pelarut tertentu, tetapi ia mestilah sama apabila mengalikan tiga faktor yang disebutkan di atas dan seterusnya memperoleh osmolariti.
Bagaimana untuk mengiranya?
Dalam kes KBR sebatian ion (dikenali sebagai kalium bromida), jika kita mempunyai satu penyelesaian dengan kepekatan 1 mol / l KBR dalam air, ia mengikuti bahawa ini mempunyai osmolarity sama dengan 2 osmol / l.
Ini disebabkan oleh sifat elektrolitnya yang kuat, yang menyokong pemisahannya yang lengkap di dalam air dan membenarkan pembebasan dua ion bebas (K+ dan Br-) yang mempunyai beberapa cas elektrik, supaya setiap tahi lalat KBr sama dengan dua osmol dalam larutan.
Secara analog, untuk penyelesaian dengan konsentrasi sama dengan 1 mol / l BaCl2 (dikenali sebagai barium klorida) dalam air, ia mempunyai osmolarity sama dengan 3 osmol / l.
Ini kerana tiga ion bebas dibebaskan: ion Ba2+ dan dua Cl ion-. Kemudian, setiap tahi lalat BaCl2 bersamaan dengan tiga osmol dalam larutan.
Sebaliknya, spesies bukan ionik tidak menjalani penyisihan sedemikian dan berasal satu osmol untuk setiap tahi lalat. Dalam kes penyelesaian glukosa dengan kepekatan sama dengan 1 mol / l, ini sama dengan 1 osmol / l penyelesaian.
Perbezaan antara osmolariti dan osmolality
An osmol ditakrifkan sebagai bilangan zarah yang larut dalam jumlah yang sama kepada 22.4 l pelarut, tertakluk kepada suhu 0 ° C dan menyebabkan generasi tekanan yang osmosis sama dengan 1 atm. Perlu diingatkan bahawa zarah-zarah ini dianggap aktif secara osmik.
Dalam pengertian ini, sifat-sifat yang dikenali sebagai osmolarity dan osmolality merujuk kepada pengukuran yang sama: kepekatan larut dalam larutan atau, meletakkan cara lain, kandungan zarah total larutan dalam larutan.
Perbezaan asas yang ditubuhkan antara osmolariti dan osmolality adalah dalam unit-unit di mana masing-masing diwakili:
Osmolarity dinyatakan dari segi jumlah bahan per isipadu larutan (iaitu osmol / l), manakala osmolaliti dinyatakan dalam jumlah bahan dengan berat badan pelarut (iaitu osmol / penyelesaian kg).
Dalam praktiknya, kedua-dua parameter digunakan dengan cara yang acuh tak acuh, bahkan memperlihatkan diri mereka dalam unit-unit yang berbeza, disebabkan oleh fakta bahawa terdapat perbezaan yang tidak dapat diaplikasikan antara jumlah magnitud dari pengukuran yang berlainan.
Rujukan
- Wikipedia. (s.f.). Kepekatan Osmotik. Diambil dari es.wikipedia.org
- Chang, R. (2007). Kimia, Edisi kesembilan. Mexico: McGraw-Hill.
- Evans, D. H. (2008). Peraturan Osmotik dan Ionik: Sel dan Haiwan. Diperoleh dari books.google.com
- Potts, W. T., dan Parry, W. (2016). Peraturan Osmotik dan Ionik dalam Haiwan. Diperoleh dari books.google.com
- Armitage, K. (2012). Siasatan secara biologi umum. Diperoleh dari books.google.com


