Struktur sulfida perak (Ag2S), sifat, nomenklatur, kegunaan
The perak sulfida adalah sebatian organik yang formula kimianya adalah Ag2S. Ia terdiri daripada pepejal hitam-kelabu yang dibentuk oleh kation Ag+ dan anion S2- dalam nisbah 2: 1. The S2- ia sangat menyerupai Ag+, kerana kedua-dua ion lembut dan mereka berjaya menstabilkan antara satu sama lain.
Perhiasan perak cenderung menggelapkan, kehilangan kilauan ciri mereka. Perubahan warna bukan produk pengoksidaan perak, tetapi tindak balasnya dengan hidrogen sulfida yang terdapat dalam persekitaran pada kepekatan rendah; Ini boleh datang dari kerosakan atau kemerosotan tumbuhan, haiwan atau makanan yang kaya dengan belerang.

The H2S, yang molekulnya membawa atom sulfur, bertindak balas dengan perak mengikut persamaan kimia berikut: 2Ag (s) + H2S (g) => Ag2S (s) + H2(g)
Oleh itu, Ag2S bertanggungjawab untuk lapisan hitam terbentuk pada perak. Walau bagaimanapun, dalam alam semula jadi sulfur ini juga boleh didapati di mineral acantita dan argentita. Kedua-dua mineral dibezakan daripada banyak lagi oleh kristal hitam dan cerah, seperti yang padat di atas imej.
The Ag2S membentangkan struktur polimorfik, sifat elektronik dan optoelektronik menarik, ia adalah semikonduktor dan berjanji untuk menjadi bahan untuk pengeluaran peranti photovoltaic seperti sel-sel solar.
Indeks
- 1 Struktur
- 2 Hartanah
- 2.1 Berat molekul
- 2.2 Penampilan
- 2.3 Bau
- 2.4 Tahap lebur
- 2.5 Kelarutan
- 2.6 Struktur
- 2.7 Indeks refraksi
- 2.8 pemalar dielektrik
- 2.9 Elektronik
- 2.10 Reaksi pengurangan
- 3 Nomenklatur
- 3.1 Sistematik
- 3.2 Saham
- 3.3 Tradisional
- 4 Kegunaan
- 5 Rujukan
Struktur
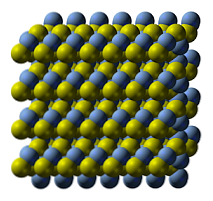
Struktur kristal silver sulfide digambarkan dalam imej atas. Bola biru sesuai dengan kation Ag+, manakala yang kuning kepada anion S2-. The Ag2S adalah polimorfik, yang bermaksud ia boleh mengguna pakai beberapa sistem kristal dalam keadaan suhu tertentu.
Bagaimana? Melalui peralihan fasa. Ion disusun semula sedemikian rupa sehingga peningkatan suhu dan getaran pepejal tidak mengganggu keseimbangan tarikan-elektrostatik. Apabila ini berlaku, dikatakan terdapat peralihan fasa, dan pepejal itu mempamerkan sifat fizikal baru (seperti kilau dan warna).
The Ag2S pada suhu normal (lebih rendah daripada 179ºC), ia mempunyai struktur kristal monoklinik (α- Ag2S). Selain fasa pepejal ini terdapat lain-lain dua: bcc (badan berpusat padu) antara 179 hingga 586ºC dan fcc (muka padu berpusat) pada suhu yang sangat tinggi (Ag δ-2S).
Mineral argentit terdiri daripada fcc fasa, juga dikenali sebagai β-Ag2S. Setelah disejukkan dan diubah menjadi tebing, ciri-ciri strukturnya diguna pakai. Oleh itu, kedua-dua struktur kristal wujud bersama: monoklinik dan bcc. Oleh itu, pepejal hitam dengan nada terang dan menarik muncul.
Hartanah
Berat molekul
247.80 g / mol
Rupa
Kristal hitam berkulit hitam
Bau
Tandas.
Titik lebur
836ºC. Nilai ini bersetuju dengan hakikat bahawa Ag2S adalah sebatian dengan watak ionik yang sedikit dan, oleh itu, cair pada suhu di bawah 1000ºC.
Kelarutan
Di dalam air hanya 6.21 ∙ 10-15 g / L pada 25ºC. Iaitu, jumlah pepejal hitam yang diselesaikan adalah diabaikan. Ini sekali lagi, disebabkan sifat kecil kutub bon Ag-S, di mana tidak terdapat perbezaan yang signifikan antara elektronegativiti antara kedua-dua atom.
Juga, Ag2S tidak larut dalam semua pelarut. Tiada molekul boleh memisahkan lapisan kristalnya dalam ion Ag+ dan S2- diselaraskan.
Struktur
Empat lapisan ikatan S-Ag-S juga boleh dilihat dalam imej struktur, yang bergerak di atas satu sama lain apabila pepejal tertakluk kepada pemahaman. Tingkah laku ini bermakna bahawa, walaupun menjadi semikonduktor, ia adalah mulur seperti banyak logam pada suhu bilik.
Lapisan S-Ag-S sesuai dengan betul kerana geometri sudutnya yang diperhatikan sebagai zigzag. Memiliki daya pemahaman, langkah ini berpindah ke paksi anjakan sehingga menyebabkan interaksi non-kovalen baru antara atom perak dan sulfur.
Indeks refraktif
2.2
Pemalar dielektrik
6
Elektronik
The Ag2S adalah semikonduktor amphoterik, iaitu, ia berkelakuan seolah-olah jenisnya n dan jenisnya p. Ia juga tidak rapuh, jadi ia telah dikaji untuk aplikasinya dalam peranti elektronik.
Tindak balas pengurangan
The Ag2S boleh dikurangkan menjadi perak metalik dengan mandi potongan hitam dengan air panas, NaOH, aluminium dan garam. Reaksi berikut berlaku:
3Ag2S (s) + 2Al (s) + 3H2O (l) => 6Ag (s) + 3H2S (ac) + Al2O3(s)
Tatanama
Perak, yang konfigurasi elektroniknya [Kr] 4d105s1, ia boleh kehilangan hanya satu elektron: iaitu 5s orbital terluarnya. Oleh itu, Agensi itu+ kekal dengan konfigurasi elektronik [Kr] 4d10. Oleh itu, ia mempunyai valensi unik +1, yang menentukan bagaimana sebatiannya harus dipanggil.
Sulfur, sebaliknya, mempunyai konfigurasi elektronik [Ne] 3s23p4, dan ia memerlukan dua elektron untuk melengkapkan oktet valensnya. Apabila ia memperoleh kedua-dua elektron (dari perak), ia berubah menjadi anion sulfur, S2-, dengan konfigurasi [Ar]. Iaitu, ia adalah isoelektronik kepada gas mulia argon.
Jadi Ag2S mesti dipanggil mengikut nomenklatur berikut:
Sistematik
Monyetsulfur diperak Di sini kita mempertimbangkan bilangan atom setiap elemen dan ditunjukkan oleh awalan pengnab Yunani.
Saham
Sulfida perak. Apabila memiliki valensi unik +1, ia tidak dinyatakan dengan angka Rom dalam kurungan: sulfida perak (I); yang tidak betul.
Tradisional
Sulfuro argentico. Oleh kerana perak "berfungsi" dengan valensi +1, akhiran -ico ditambahkan kepada namanya argentum dalam bahasa Latin.
Kegunaan
Beberapa kegunaan baru untuk Ag2S adalah yang berikut:
-Koloid nanoparticle (dengan saiz yang berbeza), penyelesaian mempunyai aktiviti anti-bakteria, tidak toksik, dan dengan itu boleh digunakan dalam bidang perubatan dan biologi.
-Nanopartikel mereka boleh membentuk apa yang dikenali sebagai titik kuantum. Ini menyerap dan memancarkan radiasi dengan intensiti yang lebih tinggi daripada banyak molekul pendarfluor organik, jadi mereka boleh menggantikannya sebagai penanda biologi.
-Struktur α-Ag2S menjadikannya mempamerkan ciri-ciri elektronik yang menarik untuk digunakan sebagai sel suria. Ia juga merupakan titik permulaan bagi sintesis bahan dan sensor termoelektrik baru.
Rujukan
- Mark Peplow. (17 April 2018). Perak sulfida semikonduktor terbentang seperti logam. Diambil dari: cen.acs.org
- Kerjasama: Penulis dan penyunting struktur kristal perak sulfida (Ag2S) III / 17E-17F-41C (). In: O. Madelung, U. Rössler, Schulz M. (ed) Bukan secara tetrahedron Berikat Elements dan Binary Compounds I. Landolt-Bornstein - pekat Matter Kumpulan III (Numerical Data dan Hubungan Kegunaan dalam Sains dan Teknologi), vol 41C. Springer, Berlin, Heidelberg.
- Wikipedia. (2018). Sulfida perak. Diambil dari: en.wikipedia.org
- Stanislav I. Sadovnikov & col. (Julai 2016). Ag2S silver sulfide nanoparticles dan penyelesaian koloid: Sintesis dan sifat. Diambil dari: sciencedirect.com
- Azo Bahan. (2018). Perak Sulfide (Ag2S) Semikonduktor. Diambil dari: azom.com
- A. Nwofe. (2015). Prospek dan cabaran filem nipis perak sulfida: Kajian semula. Bahagian Sains Bahan & Tenaga Diperbaharui, Jabatan Fizik Industri, Universiti Negeri Ebonyi, Abakaliki, Nigeria.
- UMassAmherst. (2011). Demonstrasi Kuliah: membersihkan perak yang terukir. Diambil dari: lecturedemos.chem.umass.edu
- Kajian. (2018). Apa itu Sulfide Perak? - Formula & Penggunaan Kimia. Diambil dari: study.com


